§ 1. Гипотеза де-Бройля. Волны де-Бройля.
§2. Соотношение неопределенностей Гейзенберга.
§3. Волновая функция и ее физический смысл.
§4. Уравнение Шредингера. Электрон в потенциальной яме.
§ 5. Линейный гармонический осциллятор
II. АТОМ ВОДОРОДА ПО РЕЗЕРФОРДУ-БОРУ
Опыты Резерфорда по рассеянию альфа-частиц.
§7. Постулаты Бора. Опыты Франка и Герца.
§ 8. Спектральные серии атома водорода.
§ 9. Теория атома водорода по Бору.
§ 10. Квантовые числа. Принцип Паули.
Строение электронных оболочек атома.
§ 11. Периодическая система элементов Менделеева.
§ 12. Общая картина возникновения спектров.
§ 13. Химические связи и строение молекул.
§14. Комбинационное рассеяние света.
§ 15. Спонтанное и индуцированное излучения.
§ 16. Оптические квантовые генераторы (лазеры).
§ 18. Энергия связи ядер и дефект масс.
§ 19. Ядерные силы. Модели ядра.
§20. Радиоактивное излучение и его свойства.
§ 21. Закон радиоактивного распада.
§ 22. Правила смещения. Альфа- и бета-распады.
§ 23. Ядерные реакции и их основные типы.
§ 25. Цепная реакция деления ядер урана.
§ 26. Реакция синтеза атомных ядер.
Проблема управляемых термоядерных реакций.
§ 28. Эволюция понятия “элементарная частица”.
§ 29. Виды взаимодействия элементарных частиц.
§ 30. Основные характеристики элементарных частиц.
§ 31. Внутренние квантовые числа.
§ 32. Кварковая модель адронов.
Французский ученый Луи де Бройль, развивая представления о двойственной корпускулярно-волновой природе света, выдвинул в 1923 году гипотезу об универсальности корпускулярно-волнового дуализма. Де Бройль утверждал, что между свойствами света и свойствами материальных частиц существует глубокая аналогия, следовательно материальные частицы обладают также двойственной природой, т.е. в определенных условиях проявляются их волновые свойства.
Как известно из оптики, квант света – фотон,
кроме энергии ![]() характеризуется
импульсом
характеризуется
импульсом ![]() :
:
![]() ;
;
так как
![]() .
Следовательно, длина волны фотона:
.
Следовательно, длина волны фотона:
![]() (1.1)
(1.1)
Де-Бройль постулировал, что частице с импульсом
![]() соответствует
длина волны:
соответствует
длина волны: ![]() (1.2)
(1.2)
Это соотношение (формула де Бройля) справедливо для любой частицы с импульсом р.
Вскоре гипотеза де Бройля была подтверждена экспериментально.
Американские физики К.Дэвиссон и Л.Джермер в 1927 г. изучали рассеяние
электронов на монокристалле никеля с помощью установки, изображенной на рис.
Пучок электронов из электронной пушки 1 направлялся на кристалл никеля 2,
рассеянные от кристалла электроны 3 улавливались специальным приемником 4,
соединенным с чувствительным гальванометром. Интенсивность отраженного пучка
определялась по силе тока, текущего через гальванометр. Опыты показали, что при
заданном угле падения электроны отражаются от поверхности кристалла под
различными углами, причем в одних направлениях наблюдаются максимумы числа
отраженных электронов, в других – минимумы, то есть наблюдалась дифракционная
картина. Это явление наблюдалось, когда длина электронной волны де Бройля
![]() имеет
порядок межатомного расстояния в кристалле. Дифракционные максимумы
соответствовали формуле Вульфа-Брэггов
имеет
порядок межатомного расстояния в кристалле. Дифракционные максимумы
соответствовали формуле Вульфа-Брэггов
![]() ,
а брэгговская длина волны оказалась в точности равной длине волны, вычисленной
по формуле (1.2).
,
а брэгговская длина волны оказалась в точности равной длине волны, вычисленной
по формуле (1.2).
Действительно, в опыте Джермера и Дэвиссона
скорость электрону сообщалась в ускоряющем электрическое поле пушки:
![]() .
Следовательно:
.
Следовательно: ![]() .
(1.3)
.
(1.3)
Поставив (1.3) в (1.2), получим: ![]() ,
,
где ![]() .
.
В обычных электронных приборах
![]() ,
следовательно, длина волны де Бройля должна иметь порядок
,
следовательно, длина волны де Бройля должна иметь порядок
![]() м,
то есть такой же, что и рентгеновские лучи, а расстояние между узлами
кристаллической решетки имеет тот же порядок:
м,
то есть такой же, что и рентгеновские лучи, а расстояние между узлами
кристаллической решетки имеет тот же порядок:
![]() .
При энергии электронов
.
При энергии электронов ![]() получался
острый максимум для угла рассеивания 50о. По условию дифракции
(формуле Вульфа-Брэггов) это соответствовало длине волны
получался
острый максимум для угла рассеивания 50о. По условию дифракции
(формуле Вульфа-Брэггов) это соответствовало длине волны
![]() и из формулы де-Бройля тоже:
и из формулы де-Бройля тоже:
![]() .
.
Позже П.С.Тартаковский и Г.Томсон исследовали прохождение быстрых электронов через тонкие металлические пленки. При этом на фотопластинках за этими пленками получалась дифракционная картина такая же, как при дифракции рентгеновских лучей на поликристаллах.
В 1949 г. В.А.Фабрикант, Л.М.Биберман и Н.Г.Сушкин осуществили опыты по дифракции электронов с очень малой силой тока в приборе, то есть каждый электрон регистрировался фотопластинкой в случайных местах. При длительной экспозиции была получена такая же дифракционная картина, как и при короткой с большой силой тока. Это означает, что волновые свойства присущи каждому электрону в отдельности, однако дифракция одного электрона не дает всей системы точек, которая получается при дифракции от потока. След одного электрона окажется лишь в одной точке, которая разрешена условием дифракции. В этом проявляется корпускулярная природа электронов, так как электрон не может расплыться. В какое именно из мест попадет электрон, говорить нельзя. Можно говорить лишь о вероятности попадания в точку пространства.
Таким образом, электрону присуща двойственная природа, т.е. он сочетает в себе свойства и частицы, и волны. Волновая природа электронов подтверждается опытами по их дифракции. Корпускулярная природа электронов проявляется в том, что электрон действует как единое целое, не дробясь на части.
Впоследствии дифракционные явления обнаружили также для нейтронов, протонов, атомных и молекулярных пучков. Это окончательно послужило доказательством наличия волновых свойств микрочастиц и позволило описать движение микрочастиц в виде волнового процесса, характеризующегося определенной длиной волны, рассчитываемой по формуле де Бройля (1.2).
Подтвержденная экспериментально гипотеза де Бройля о корпускулярно-волновом дуализме свойств вещества коренным образом изменила представления о свойствах микрообъектов. Всем микрообъектам присущи и корпускулярные, и волновые свойства; в то же время любую из микрочастиц нельзя считать ни частицей, ни волной в классическом понимании.
В.Гейзенберг, учитывая волновые свойства
микрочастиц и связанные с волновыми свойствами ограничения в их поведении,
пришел в 1927 г. к выводу, что объект микромира невозможно одновременно с любой
наперед заданной точностью характеризовать и координатой и импульсом. Согласно
соотношению неопределенностей Гейзенберга, микрочастица не может
иметь одновременно и определенную координату (х, у,
z),
и определенную соответствующую проекцию импульса (рх, ру,
pz),
причем неопределенности этих величин удовлетворяют условиям:
![]() ,
,
![]() ,
,
![]() ,
(2.1)
,
(2.1)
где Dx,
Dу,
Dz
– неопределенности координат частицы, а
![]() ,
,
![]() ,
,
![]() -
неопределенности компонент импульса. Произведение неопределенностей координаты и
соответствующей ей проекции импульса не может быть меньше величины порядка
h.
То есть, чем точнее мы знаем
координату, тем менее определена проекция импульса и наоборот. Отсюда вытекает и
фактическая невозможность одновременно с любой, наперед заданной точностью
измерить координату и импульс микрообъекта.
-
неопределенности компонент импульса. Произведение неопределенностей координаты и
соответствующей ей проекции импульса не может быть меньше величины порядка
h.
То есть, чем точнее мы знаем
координату, тем менее определена проекция импульса и наоборот. Отсюда вытекает и
фактическая невозможность одновременно с любой, наперед заданной точностью
измерить координату и импульс микрообъекта.
Поясним, что соотношение неопределенностей действительно вытекает из волновых свойств микрочастиц. Пусть поток электронов проходит через узкую щель шириной Dх, расположенную перпендикулярно направлению их движения (рис.2.1). Так как электроны обладают волновыми свойствами, то при их прохождении через щель, размер которой сравним с длиной волны де Бройля l электрона, наблюдается дифракция. Дифракционная картина, наблюдаемая на экране (Э), характеризуется главным максимумом, расположенным симметрично оси Y, и побочными максимумами по обе стороны от главного (их не рассматриваем из-за незначительной интенсивности по сравнению с главным максимумом).
До прохождения через щель электроны двигались вдоль оси
Y,
поэтому составляющая импульса рх=0, так что
![]() =0,
а координата х частицы является совершенно неопределенной. В момент
прохождения электронов через щель их положение в направление оси Х определяется
с точностью до ширины щели, т.е. с точностью
Dх.
В этот же момент вследствие дифракции электроны отклоняются от первоначального
направления и будут двигаться в пределах угла 2j
(j
– угол, соответствующий первому дифракционному минимуму). Следовательно,
появляется неопределенность в значении составляющей импульса вдоль оси
Y,
которая, как следует из рис.2.1 и формулы (1.2), равна
=0,
а координата х частицы является совершенно неопределенной. В момент
прохождения электронов через щель их положение в направление оси Х определяется
с точностью до ширины щели, т.е. с точностью
Dх.
В этот же момент вследствие дифракции электроны отклоняются от первоначального
направления и будут двигаться в пределах угла 2j
(j
– угол, соответствующий первому дифракционному минимуму). Следовательно,
появляется неопределенность в значении составляющей импульса вдоль оси
Y,
которая, как следует из рис.2.1 и формулы (1.2), равна
![]() .
(2.2)
.
(2.2)
Ограничимся рассмотрением электронов, попадающих на экран в пределах главного максимума. Из теории дифракции известно, что первый минимум соответствует углу j, удовлетворяющему условию
![]() ,
(2.3)
,
(2.3)
где
Dх–ширина щели, а
l
– длина волны де Бройля. Из формул (2.2) и (2.3) получим
![]() ,
,
где учтено, что для некоторой
незначительной части электронов, попадающих за пределы главного максимума,
![]() .
Следовательно, получаем выражение
.
Следовательно, получаем выражение
![]() ,
то есть соотношение неопределенностей (2.1).
,
то есть соотношение неопределенностей (2.1).
Соотношение неопределенностей получено при одновременном использовании классических характеристик движения частицы (координаты, импульса) и наличия у нее волновых свойств. Оно является квантовым ограничением применимости классической механики к микрообъектам и позволяет оценить, например, в какой мере можно применять понятия классической механики к микрочастицам, в частности, с какой степенью точности можно говорить о траекториях микрочастиц. Известно, что движение по траектории характеризуется в любой момент времени определенными значениями координат и скорости. Выразим соотношение неопределенностей (2.1) в виде
![]() (2.4)
(2.4)
Из этого выражения следует, что чем больше масса частицы, тем меньше неопределенности ее координаты и скорости и, следовательно, с тем большей точностью можно применять к этой частице понятие траектории. Для описания движения макротел с абсолютной достоверностью можно пользоваться законами классической механики, чего нельзя делать для описания, например, движения электрона в атоме.
В квантовой теории рассматривается также соотношение неопределенностей для энергии Е и времени t, т.е. неопределенности этих величин удовлетворяют условию
![]() (4.5)
(4.5)
где DЕ – неопределенность энергии некоторого состояния системы, Dt – промежуток времени, в течение которого оно существует. Следовательно, система, имеющая среднее время жизни Dt, не может быть охарактеризована определенным значением энергии; разброс энергии DЕ=h/Dt возрастает с уменьшением среднего времени жизни. Из выражения (4.5) следует, что частота излученного фотона также должна иметь неопределенность Dn =DЕ /h, т.е. линии спектра должны характеризоваться частотой, равной n±DЕ /h. Опыт действительно показывает, что все спектральные линии размыты; измеряя ширину спектральной линии, можно оценить порядок времени существования атома в возбужденном состоянии.
Из содержания предыдущих двух параграфов следует, что с микрочастицей сопоставляют волновой процесс, который соответствует ее движению, поэтому состояние частицы в квантовой механике описывают волновой функцией, которая зависит от координат и времени y(x,y,z,t). Конкретный вид y-функции определяется состоянием частицы, характером действующих на нее сил. Если силовое поле, действующее на частицу, является стационарным, т.е. не зависящим от времени, то y-функцию можно представить в виде произведения двух сомножителей, один из которых зависит от времени, а другой – от координат:
![]() (3.1)
(3.1)
В дальнейшем будем рассматривать только стационарные состояния.
y-функция является вероятностной
характеристикой состояния частицы.
Чтобы пояснить это, мысленно выделим достаточно малый объем
![]() , в пределах которого значения
y-функции будем считать
одинаковыми. Тогда вероятность нахождения
dW
частицы в данном объеме
пропорциональна ему и зависит от квадрата модуля
y-функции
(квадрата модуля амплитуды волн де Бройля):
, в пределах которого значения
y-функции будем считать
одинаковыми. Тогда вероятность нахождения
dW
частицы в данном объеме
пропорциональна ему и зависит от квадрата модуля
y-функции
(квадрата модуля амплитуды волн де Бройля):
![]() (3.2)
(3.2)
Отсюда следует физический смысл волновой функции:
![]() .
(3.3)
.
(3.3)
Квадрат модуля волновой функции имеет смысл плотности вероятности, т.е. определяет вероятность нахождения частицы в единичном объеме в окрестности точки с координатами х, у, z.
Интегрируя выражение (3.2) по объему, определяем вероятность нахождения частицы в этом объеме в условиях стационарного поля:
![]() (3.4)
(3.4)
Если известно, что частица находится в пределах объема V, то интеграл выражения (3.4), взятый по объему V, должен быть равен единице:
![]() (3.5)
(3.5)
– условие нормировки y-функции.
Чтобы волновая функция являлась объективной характеристикой состояния микрочастиц, она должна быть конечной, однозначной, непрерывной, так как вероятность не может быть больше единицы, не может быть неоднозначной величиной и не может изменяться скачками. Таким образом, состояние микрочастицы полностью определяется волновой функцией. Частица может быть обнаружена в любой точке пространства, в которой волновая функция отлична от нуля.
Основной характеристикой состояния атомов, молекул, элементарных частиц является y-функция. Аналитическое выражение y-функции в каждом конкретном случае можно получить путем решения волнового уравнения – основного уравнения квантовой механики, предложенного Э. Шредингерам в 1920 г.
Применительно к стационарным состояниям уравнение Шредингера имеет вид:
![]() .
(4.1)
.
(4.1)
где т – масса частицы; Е и U – ее полная и потенциальная энергии.
Если частица перемещается только вдоль некоторой линии, например, вдоль оси ОХ (одномерный случай), то уравнение Шрёдингера упрощается и принимает вид:
![]() (4.2)
(4.2)
Одним из наиболее простых примеров использования уравнения Шрёдингера является решение задачи о движении частицы в одномерной потенциальной яме.
Пусть электрон перемещается вдоль оси ОХ только в пределах 0<х<l (рис. 4.1). Это означает, что в указанном интервале y-функция отлична от нуля, а вне интервала (х < 0, х³ l) равна нулю.
Так как на частицу в выделенном интервале силовые поля не действуют, то ее потенциальная энергия может иметь любое постоянное значение (наиболее удобно принять U=0). Вне этого интервала электрона нет, поэтому следует считать его потенциальную энергию бесконечно большой. На рис. 4.1 показана графическая зависимость U = f(x). Интервал 0<х<l, удовлетворяющий сформулированным выше условиям, называют одномерной прямоугольной потенциальной ямой с бесконечно высокими стенками. С учетом U=0 уравнение Шрёдингера (4.2) для интервала 0<х<l имеет вид:
![]() .
(4.3)
.
(4.3)
Введем обозначение: ![]() ,
(4.4)
,
(4.4)
тогда:
![]() (4.5)
(4.5)
Это уравнение аналогично дифференциальному уравнению гармонического колебания, решение которого:
![]() ,
(4.10)
,
(4.10)
где
![]() –амплитуда
волновой функции,
–амплитуда
волновой функции, ![]() –ее
начальная фаза. Чтобы найти две постоянные
–ее
начальная фаза. Чтобы найти две постоянные
![]() и
и
![]() ,
а также возможные значения
,
а также возможные значения ![]() или
Е, рассмотрим граничные условия:
или
Е, рассмотрим граничные условия:
1) при х =0 y = 0. Подставляя эти значения в (4.10), получаем
![]()
Физический смысл здесь имеет только одно значение:
![]() =
0, откуда
=
0, откуда ![]() .
.
2)
при х =l
y = 0.
C учетом
![]() из
(4.10) имеем:
из
(4.10) имеем:
![]()
Физический смысл здесь имеет только одно значение:
![]() ,
или
,
или ![]() ,
откуда
,
откуда
![]() ,
(4.7)
,
(4.7)
где п –
целое число, оно принимает значения 1, 2, 3, ...; п ≠ 0, так как в
противном случае
y= 0
при любом х, что означает отсутствие электрона в потенциальной яме. Число
n
называют квантовым числом. Из (4.4) находим энергию
![]() ,
что с учетом (4.7) дает:
,
что с учетом (4.7) дает:
![]() .
(4.8)
.
(4.8)
Индекс n при Е показывает, что различным значениям квантового числа n соответствует и разная энергия.
Подставляя
w
(4.7) в (4.5) и учитывая ![]() ,
получаем
,
получаем
![]() .
(4.9)
.
(4.9)
Из (4.8) следует, что решение уравнения
Шредингера для электрона в потенциальной
яме без каких-либо дополнительных постулатов приводит к
дискретным, квантованным значениям энергии: ![]() ;
;
![]() и
т.д.
и
т.д.
Возведя (4.9) в квадрат, получим плотность вероятности
![]() нахождения
электрона
в разных точках потенциальной ямы. На рис.4.2. показана графическая зависимость
нахождения
электрона
в разных точках потенциальной ямы. На рис.4.2. показана графическая зависимость
![]() от
х при разных дискретных состояниях, то есть разных квантовых числах. Как
видно из рисунка, электрон может с разной с разной вероятностью находиться в
разных местах потенциальной ямы. Есть такие точки,
в которых вероятность нахождения электрона вообще равна нулю.
Это существенно отличается от
представлений классической физики, согласно
которым равновероятно нахождение
частицы в разных местах потенциальной ямы
от
х при разных дискретных состояниях, то есть разных квантовых числах. Как
видно из рисунка, электрон может с разной с разной вероятностью находиться в
разных местах потенциальной ямы. Есть такие точки,
в которых вероятность нахождения электрона вообще равна нулю.
Это существенно отличается от
представлений классической физики, согласно
которым равновероятно нахождение
частицы в разных местах потенциальной ямы
Линейный гармонический осциллятор – это система, совершающая одномерное движение под действием квазиупругой силы. Он является моделью, используемой во многих задачах классической и квантовой теории. Пружинный, физический и математический маятники – примеры классических гармонических осцилляторов. Потенциальная энергия гармонического осциллятора равна:
![]() ,
(5.1)
,
(5.1)
где
![]() —
собственная частота колебаний осциллятора, т — масса частицы. Зависимость (5.1) имеет вид параболы (рис. 5.1), т.е. «потенциальная яма» в
данном случае
является параболической.
Амплитуда малых колебаний классического осциллятора определяется его полной
энергией Е. В точках с
координатами ±хmax
полная энергия Е
равна
потенциальной
энергии. Поэтому с классической точки зрения частица не может выйти
за
пределы области
—
собственная частота колебаний осциллятора, т — масса частицы. Зависимость (5.1) имеет вид параболы (рис. 5.1), т.е. «потенциальная яма» в
данном случае
является параболической.
Амплитуда малых колебаний классического осциллятора определяется его полной
энергией Е. В точках с
координатами ±хmax
полная энергия Е
равна
потенциальной
энергии. Поэтому с классической точки зрения частица не может выйти
за
пределы области
(–хmax,+ хmax).
Гармонический осциллятор в квантовой механике – квантовый осциллятор – описывается уравнением Шредингера (4.2), учитывающим выражение (5.1) для потенциальной энергии. Тогда стационарные состояния квантового осциллятора определяются уравнением Шредингера вида
![]() (5.2)
(5.2)
где Е — полная энергия осциллятора. В теории дифференциальных уравнений доказывается, что уравнение (5.2) решается только при собственных значениях энергии
![]() (5.3)
(5.3)
где
![]() .
Формула (5.3)
показывает, что энергия квантового осциллятора может иметь лишь
дискретные значения, т.е. квантуется.
Энергия ограничена снизу отличным от нуля
минимальным значением энергии
.
Формула (5.3)
показывает, что энергия квантового осциллятора может иметь лишь
дискретные значения, т.е. квантуется.
Энергия ограничена снизу отличным от нуля
минимальным значением энергии
![]() .
Существование минимальной энергии, называемой энергией нулевых колебаний, представляет собой прямое следствие соотношения неопределенностей.
.
Существование минимальной энергии, называемой энергией нулевых колебаний, представляет собой прямое следствие соотношения неопределенностей.
Наличие нулевых колебаний означает, что частица не может находиться на дне «потенциальной ямы», причем этот вывод не зависит от ее формы. В самом деле, «падение на дно ямы» связано с обращением в нуль импульса частицы, а вместе с тем и его неопределенности. Тогда неопределенность координаты становится сколь угодно большой, что противоречит, в свою очередь, пребыванию частицы в «потенциальной яме».
Вывод о наличии энергии нулевых колебаний квантового осциллятора противоречит выводам классической теории. Например, классическая физика приводит к выводу, что при Т=0 К (Ек=0) энергия колебательного движения атомов кристалла должна обращаться в нуль. Однако эксперименты по рассеянию света показывают, что при Т®0 колебания атомов в кристалле не прекращаются.
Из формулы (5.3) также следует, что
уровни энергии линейного гармонического осциллятора расположены на одинаковых
расстояниях друг от друга (рис. 5.2), а именно
расстояние между соседними энергетическими уровнями равно
![]() ,
причем минимальное
значение энергии ½
,
причем минимальное
значение энергии ½![]() .
.
Квантово-механический расчет
показывает, что
частицу можно обнаружить за пределами дозволенной области
(–хmax, + хmax),
в то время как с классической точки зрения она не может выйти
за ее пределы.
Следовательно, имеется отличная от нуля вероятность
обнаружить частицу в той области, которая является классически запрещенной. Этот
результат (без вывода) демонстрируется на рис.5.3, где приводится квантовая
плотность вероятности
![]() обнаружения
осциллятора для состояния п=1. Из рисунка
следует, что для квантового осциллятора действительно плотность вероятности
имеет конечные значения за пределами классически дозволенной области |x|³ хmax,
т.е. имеется конечная
(но
небольшая)
вероятность обнаружить частицу за пределами «потенциальной ямы».
обнаружения
осциллятора для состояния п=1. Из рисунка
следует, что для квантового осциллятора действительно плотность вероятности
имеет конечные значения за пределами классически дозволенной области |x|³ хmax,
т.е. имеется конечная
(но
небольшая)
вероятность обнаружить частицу за пределами «потенциальной ямы».
II. АТОМ ВОДОРОДА ПО РЕЗЕРФОРДУ-БОРУ
До конца ХIХ века считалось, что атомы – мельчайшие неделимые частицы вещества. Но открытие электрона показало, что эта отрицательно заряженная частица почти в 2000 раз легче атома и входит в состав любых атомов.
При различных процессах атомы теряют электроны и превращаются в положительно заряженные ионы. Это означает, что атомы – сложные образования и состоят из положительно заряженных частиц и электронов. Как распределены эти частицы в атоме – было не известно.
Первая попытка создания модели атома принадлежит Дж. Дж. Томсону (1903). Согласно этой модели, атом представляет собой непрерывно заряженный положительным зарядом шар с радиусом порядка 10–10 м, внутри которого около своих положений равновесия колеблются электроны. Суммарный отрицательный заряд электронов равен положительному заряду шара, поэтому атом в целом нейтрален. равномерно распределенным положительным зарядом и внутри сферы находятся электроны. Позднее было доказано, что представление о непрерывно распределенном внутри атома положительном заряде ошибочно.
В 1910-1911 гг. Э. Резерфорд с сотрудниками (Г. Гейгер и Э. Марсденн) провел опыты по зондированию атомов с целью выяснения характера распределения положительных и отрицательных зарядов в атоме. Для этого узкий пучок a - частиц, испускаемых радиоактивным веществом Р, направлялся на тонкую металлическую фольгу Ф, за ней помещался экран Э, который был покрыт сернистым цинком и при соударение с a-частицами экран светился. Вызываемые ударами a-частиц вспышки света наблюдались в микроскоп М. Микроскоп и экран можно было вращать вокруг оси, проходящей через центр рассеивающей фольги.
Напомним,
a-частицы
– это частицы, которые испускаются некоторыми радиоактивными элементами. Они
обладают положительным зарядом, равным удвоенному элементарному заряду и
движутся со скоростью ![]() =107 м/с, поэтому обладают большой проникающей
способностью.
=107 м/с, поэтому обладают большой проникающей
способностью.
Опыты показали, что a-частицы, пролетая через фольгу, рассеивались на разные углы. В некоторых случаях угол рассеивания j превышал 900. Объяснить это можно было взаимодействием a - частиц с положительным зарядом атома. Причем этот заряд должен занимать малый объем и обладать большой массой. На основании этих опытов Резерфорд предложил ядерную модель строения атома. Согласно Резерфорду атом представляет собой систему зарядов, в центре которой расположено тяжелое положительное ядро с зарядом Ze, имеющей размеры, не превышающие 10-14 м, а вокруг ядра расположены Z электронов, распределенных по всему объему, занимаемому атомом. Почти вся масса атома сосредоточена в ядре.
Однако ядерная модель оказалась в противоречии с законами классической механики и электродинамики. Поскольку система неподвижных зарядов не может находиться в устойчивом состоянии, Э.Резерфорду пришлось отказаться от статической модели атома и предположить, что электроны движутся вокруг ядра, описывая искривленные траектории. Но в этом случае электрон будет двигаться с ускорением, в связи с чем, согласно классической электродинамике, он должен непрерывно излучать электромагнитные (световые) волны и иметь сплошной спектр излучения. Процесс излучения сопровождается потерей энергии, так что электрон должен, в конечном счете, упасть на ядро. Из опыта известно, что атомы – это устойчивые образования, а спектр их излучения линейчатый, а не сплошной.
Для объяснения противоречий модели строения атома опытным фактам датский физик Нильс Бор в 1913 г. обобщил гипотезу Планка для любой атомной системы, положив тем самым начало развитию квантовой теории строения атома. В основе теории Бора лежат два постулата:
I. Атомы и атомные системы могут длительное время находиться в определенных состояниях, называемых стационарными, при этом атом не излучает и не поглощает энергию. Энергии стационарных состояний образуют дискретный ряд Е1, Е2, Е3,…
II. Атомы излучают или поглощают энергию при переходе из одного стационарного состояния в другое, при этом квант излучаемой или поглощаемой энергии определяется соотношением: hv=En–Em , где En , Em – энергии стационарных состояний, между которыми произошел переход.
Данные постулаты экспериментально были подтверждены опытами немецких
физиков Дж. Франка и Г. Герца. В трубке, заполненной парами ртути при малом
давлении (давление приблизительно равно 13 Па) содержатся катод (К), две
сетки (С1 и С2), анод (А). Исследовалась зависимость силы
тока
I
от ускоряющего потенциала
U
между катодом и сеткой С1. Электроны, вылетающие из катода за счет
термоэлектронной эмиссии, разгонялись в электрическом поле между катодом и
сеткой С1, приобретая энергию
![]() .
Между сеткой С2 и анодом приложен небольшой (примерно 0,5 В)
задерживающий потенциал. Электроны, ускоренные в области 1, попадают в
область 2 между сетками, где испытывают соударения с атомами паров ртути.
Электроны, которые после соударений имеют достаточную энергию для преодоления
задерживающего потенциала в области 3, достигают анода.
.
Между сеткой С2 и анодом приложен небольшой (примерно 0,5 В)
задерживающий потенциал. Электроны, ускоренные в области 1, попадают в
область 2 между сетками, где испытывают соударения с атомами паров ртути.
Электроны, которые после соударений имеют достаточную энергию для преодоления
задерживающего потенциала в области 3, достигают анода.
При увеличении ускоряющего потенциала от 0 до 4,9 В гальванометр показал
монотонный рост анодного тока. При значениях
U³4,9
В ( и кратных ему значениях
U³
9,8 В; 14,7 В;…) на кривой
I(U)
появляются спады (рис.7.2). Это объясняется тем, что атомы ртути могут
находиться только в состоянии с энергиями
E1,
Е2, Е3, и т.д., а воспринимают энергию
DЕ=
Е2– Е1. В данном случае
DЕ=4,9
эВ (электронвольт). Пока энергия электрона
![]() ,
соударения электронов с атомами упругие, т.е. электрон при
соударении не теряет энергию. Поэтому он преодолевает тормозящее поле в области
3 и долетает до анода (ток растет). При
,
соударения электронов с атомами упругие, т.е. электрон при
соударении не теряет энергию. Поэтому он преодолевает тормозящее поле в области
3 и долетает до анода (ток растет). При ![]() =4,9
эВ соударение электрона с атомом ртути неупругое. Электрон отдает энергию
атому и не может преодолеть тормозящее поле. Ток падает.
=4,9
эВ соударение электрона с атомом ртути неупругое. Электрон отдает энергию
атому и не может преодолеть тормозящее поле. Ток падает.
Таким образом, опыты
Франка и Герца показали, что электроны при столкновении с атомами ртути передают
атомам только определенные порции энергии, причем 4,9 эВ – наименьшая возможная
порция энергии (наименьший квант энергии), которая может быть поглощена атомом
ртути в основном энергетическом состоянии. Атом ртути при этом переходит в новое
стационарное состояние (возбужденное). В этом состоянии атом может находиться
время Dt
»
10-8 c,
после чего вновь возвращается в состояние с энергией Е1, испуская
квант с частотой ![]() .
Значение длины волны
l=с/u=253,7
нм оказалось в соответствии со вторым постулатом Бора:
.
Значение длины волны
l=с/u=253,7
нм оказалось в соответствии со вторым постулатом Бора:
![]() ,
где Е1, Е2–энергии основного и возбужденного
уровней энергии. Следовательно, идея Бора о существовании в атомах
стационарных состояний блестяще выдержала экспериментальную проверку.
,
где Е1, Е2–энергии основного и возбужденного
уровней энергии. Следовательно, идея Бора о существовании в атомах
стационарных состояний блестяще выдержала экспериментальную проверку.
Исследования спектров излучения разреженных газов (т.е. спектров излучения отдельных атомов) показали, что каждому газу присущ определенный линейчатый спектр, состоящий из отдельных спектральных линий или групп близко расположенных линий. Особенно отчетливо это проявляется в спектре простейшего атома водорода.
Швейцарский ученый И.Бальмер подобрал эмпирическую формулу, описывающую все известные в то время спектральные линии атома водорода в видимой области спектра:
![]() (8.1).
(8.1).
где В=const, n=3;4;5;6.
Если введем обозначение
![]() -
волновое число, тогда:
-
волновое число, тогда:
![]() (8.2),
(8.2),
где ![]() =1,10.107
м-1 – постоянная Ридберга.
=1,10.107
м-1 – постоянная Ридберга.
Из выражений (8.1) и (8.2) вытекает, что спектральные линии, отличающиеся различными значениями n, образуют группу или серию линий, называемую серией Бальмера:
![]() (8.3),
(8.3),
где n=3;4;5;6.
С увеличением
n
линии серии сближаются; волновые числа
![]() (при n®¥),
(при n®¥),
![]()
![]() определяют
границы спектральной серии.
определяют
границы спектральной серии.
Наряду с серией Бальмера в спектре атомарного водорода были обнаружены другие серии, волновые числа которых можно представить аналогичными формулами.
В ультрафиолетовой области серия Лаймана:
![]() n
= 2;3… (8.4)
n
= 2;3… (8.4)
В инфракрасной области:
![]() - серия Пашена,
n
=4;5…
- серия Пашена,
n
=4;5…
![]() )
- серия Брэкета, n
= 5;6… (8.5)
)
- серия Брэкета, n
= 5;6… (8.5)
![]() - серия Пфунда,
n
= 6;7…
- серия Пфунда,
n
= 6;7…
![]() - серия Хемфри,
n
= 7;8…
- серия Хемфри,
n
= 7;8…
Анализируя соотношения (8.3) – (8.5), можно сказать, что все серии атомарного водорода можно представить общей формулой, называемой обобщенной формулой Бальмера:
![]() (8.6)
(8.6)
где m
имеет в каждой данной серии постоянное значение,
m=1;2;3;4;5;6
(определяет серию); а n=m+1,
m+2,…
(определяет отдельные линии этой серии). Обозначим величины
![]() и
и
![]() –
спектральные термы. Тогда (8.6) запишется
–
спектральные термы. Тогда (8.6) запишется
![]() (8.7).
(8.7).
Соотношение (8.7) получило название комбинационный принцип.
Этот принцип был установлен опытным путем, а
теория Бора дала ему толкование: каждому спектральному терму соответствует
определенное стационарное состояние атома и 2–ой постулат Бора – это есть
комбинационный принцип, выраженный иным способом. Действительно, т.к.
![]() ,
а
,
а ![]() ,
то
,
то ![]() .
По второму постулату Бора
.
По второму постулату Бора ![]() или
или
![]() ,
,
![]() (8.8).
(8.8).
Сравнивая (8.7) и (8.8) можно записать:
![]() и
и
![]() .
.
Отсюда получается выражение для энергии стационарного состояния атома: ![]() (8.9)
(8.9)
Знак «–» имеет условное значение, чисто физический смысл – энергия электрона в поле положительного ядра отрицательна. Из (8.9) видно, что энергия стационарных состояний образует дискретный ряд при n=1;2;3…
Постулаты, выдвинутые Бором, позволили рассчитать спектр атома водорода и водородоподобных систем (систем, состоящих из ядра с зарядом Ze и одного электрона (например, ионы Не+, Li+), а также теоретически вычислить постоянную Ридберга.
Следуя Бору, рассмотрим движение электрона в водородоподобной системе, ограничиваясь круговыми стационарными орбитами. Потенциальная энергия взаимодействия электрона с ядром:
![]() (9.1),
(9.1),
r
– радиус орбиты. Кинетическая энергия электрона, движущего вокруг ядра: ![]() (9.2).
(9.2).
Тогда полная энергия атома:
![]() (9.3).
(9.3).
Электрон вокруг ядра движется с ускорением
![]() под
действием кулоновской силы:
под
действием кулоновской силы:
![]() .
.
По второму закону Ньютона (ma = Fk) можно записать:
![]() (9.4);
(9.4);
отсюда
![]() (9.5).
(9.5).
Поставим (9.5) в (9.3):
![]() (9.6).
(9.6).
По классической механике радиус орбиты электрона может принимать любые значения, тогда и энергия согласно (9.6) может принимать любые значения. Согласно же постулатам Бора энергия атома, а значит и радиус орбиты электрона определенные. Бор предложил правило отбора или правило квантования (третий постулат Бора): из всех возможных орбит электрона осуществляется только те, для которых момент импульса электрона кратен постоянной Планка:
![]() (9.7),
(9.7),
где n=1,2,3,… – главное квантовое число. Используя соотношения (9.4) и (9.7) определим радиус стационарной орбиты электрона:
![]()
![]() (9.8),
(9.8),
при ![]() (радиус
первой орбиты).
(радиус
первой орбиты).
Из (9.8) следует ![]() . Подставляя (9.8) в (9.10) получим выражение для энергии
стационарных состояний:
. Подставляя (9.8) в (9.10) получим выражение для энергии
стационарных состояний:
![]() =
=![]() (9.9)
(9.9)
При ![]() –
энергия первого стационарного состояния.
–
энергия первого стационарного состояния.
В состоянии с энергией Е1 атом может находиться сколь угодно долго. Для того, чтобы ионизировать атом водорода, т.е. оторвать от него электрон, ему нужно сообщить энергию 13,55 эВ.
![]() эВ;
эВ;
![]() ;
;
![]() эВ;
эВ;
![]() эВ;
эВ;
![]() эВ
и т.д.
эВ
и т.д.
Состояние
![]() ,
,
![]() ,…
соответствуют возбужденному атому. Время жизни в этих состояниях имеет порядок
,…
соответствуют возбужденному атому. Время жизни в этих состояниях имеет порядок
![]() . За это время электрон успевает совершить около 100 млн. оборотов
вокруг ядра.
. За это время электрон успевает совершить около 100 млн. оборотов
вокруг ядра.
Придавая n различные целочисленные значения, получим для атома водорода, согласно формуле (9.9), возможные уровни энергии. Энергия атома водорода с увеличением п возрастает и энергетические уровни сближаются к границе, соответствующей значению п=¥. Атом водорода обладает, таким образом, минимальной энергией (Е1=–13,55 эВ) при n=1 и максимальной (Е¥=0) при п=¥. Следовательно, значение Е¥=0 соответствует ионизации атома (отрыву от него электрона). Согласно второму постулату Бора, при переходе атома водорода из стационарного состояния n в стационарное состояние т с меньшей энергией испускается квант:
![]()
![]() ,
,
откуда частота излучения:
![]()
![]() =R
=R![]() ,
(9.10)
,
(9.10)
где
![]() .
.
Воспользовавшись при вычислении
R
современными значениями универсальных постоянных, получим величину, совпадающую
с экспериментальным значением постоянной Ридберга в эмпирических формулах для
атома водорода: ![]() .
.
Это совпадение доказывает правильность полученной Бором формулы для энергетических уровней водородоподобной системы.
Подставляя, например, в формулу (9.10) т=1 и п=2, 3, 4, ..., получим группу линий, образующих серию Лаймана и соответствующих переходам электронов с возбужденных уровней (п=2, 3, 4, ...) на основной (т=1). Аналогично, при подстановке т=2, 3, 4, 5, 10 и соответствующих им значений n получим серии Бальмера, Пашена, Брэкета, Пфунда и Хэмфри (часть из них схематически представлена на рис.9.1.). Следовательно, по теории Бора, количественно объяснившей спектр атома водорода, спектральные серии соответствуют излучению, возникающему в результате перехода атома в данное состояние из возбужденных состояний, расположенных выше данного.
 Теория Бора показала неприменимость классической физики к внутриатомным
явлениям и необходимость применения квантовых законов в микромире. Но попытка
построить аналогичную теорию для атома гелия потерпела неудачу. Теория Бора не
была ни последовательно классической, ни последовательно квантовой теорией.
Недостатки теории Бора могли быть устранены путем создания новой квантовой
теории, в которой поведение и движение микрочастиц подчиняется своим законам.
Это было осуществлено при создании квантовой механики.
Теория Бора показала неприменимость классической физики к внутриатомным
явлениям и необходимость применения квантовых законов в микромире. Но попытка
построить аналогичную теорию для атома гелия потерпела неудачу. Теория Бора не
была ни последовательно классической, ни последовательно квантовой теорией.
Недостатки теории Бора могли быть устранены путем создания новой квантовой
теории, в которой поведение и движение микрочастиц подчиняется своим законам.
Это было осуществлено при создании квантовой механики.
Состояние электрона в атоме характеризуется не одним, а несколькими квантовыми числами.
Первое
их квантовых чисел – главное квантовое число: n =1; 2;3,…
Оно определяет уровни энергии электрона в атоме:
![]() и радиусы стационарных орбит
и радиусы стационарных орбит
![]() . Эти выражения вытекают из решения уравнения Шредингера и совпадают
с соответствующими формулами, полученными Бором.
. Эти выражения вытекают из решения уравнения Шредингера и совпадают
с соответствующими формулами, полученными Бором.
Второе
квантовое число – орбитальное квантовое число
![]() ,
которое при данном n
может
принимать
значения 0, 1, 2, ...,
n–1
. Это число определяет орбитальный момент
импульса
,
которое при данном n
может
принимать
значения 0, 1, 2, ...,
n–1
. Это число определяет орбитальный момент
импульса![]() электрона
относительно ядра. Момент импульса электрона в атоме квантуется по формуле:
электрона
относительно ядра. Момент импульса электрона в атоме квантуется по формуле:
![]()
Третье
квантовое число – магнитное квантовое число
![]() ,
которое при данном
,
которое при данном ![]() принимает
значения
0;
±1; ±2,…,
±
принимает
значения
0;
±1; ±2,…,
±![]() ;
всего 2
;
всего 2![]() +1
значений. Это число определяет проекции
орбитального момента импульса электрона на некоторое произвольно выбранное
направление Z.
Возможны лишь такие ориентации вектора момента импульса
+1
значений. Это число определяет проекции
орбитального момента импульса электрона на некоторое произвольно выбранное
направление Z.
Возможны лишь такие ориентации вектора момента импульса
![]() ,
при которых проекция
,
при которых проекция ![]() вектора
вектора
![]() на
направление внешнего магнитного поля (ось OZ)
принимает значения:
на
направление внешнего магнитного поля (ось OZ)
принимает значения:
![]()
Четвертое
квантовое число – спиновое (магнитное спиновое)
квантовое число ms.
Оно может принимать только
два значения
![]() и
характеризует возможные значения проекции на ось Z спина (собственного
механического момента импульса)
и
характеризует возможные значения проекции на ось Z спина (собственного
механического момента импульса)
![]() электрона:
электрона:
![]() ,
где
,
где ![]() –
спиновое квантовое число. Пространственное квантование спина означает, что
проекция
–
спиновое квантовое число. Пространственное квантование спина означает, что
проекция
![]() вектора
спина
вектора
спина ![]() на
направление внешнего магнитного поля находится по формуле:
на
направление внешнего магнитного поля находится по формуле:
![]() .
.
В 1924 г. швейцарский физик Паули сформулировал
принцип, согласно которому: в любом атоме не может быть двух электронов,
находящихся в двух одинаковых стационарных состояниях, определяемых набором
четырех квантовых чисел – главного n; орбитального
![]() ;
магнитного m и спинового ms. Принципу Паули, кроме
электронов подчиняются другие частицы, имеющие полуцелый спин (в единицах
;
магнитного m и спинового ms. Принципу Паули, кроме
электронов подчиняются другие частицы, имеющие полуцелый спин (в единицах
![]() ).
).
Для электронов в атоме принцип Паули записывается
таким образом: ![]() или
1,
или
1,
где ![]() –число
электронов в состоянии, характеризуемом данным набором квантовых чисел.
–число
электронов в состоянии, характеризуемом данным набором квантовых чисел.
Максимальное число электронов, находящихся
в состояниях, описываемых набором трех квантовых чисел n;
![]() и
m и отличающихся только ориентацией спинов электронов, равно
и
m и отличающихся только ориентацией спинов электронов, равно
![]() =2,
=2,
т.к. ms принимает два значения, т.е.
±1/2.
Можно сказать: не может быть больше двух электронов, движение которых
характеризуется одинаковыми значениями трех квантовых чисел n;
![]() и
m.
и
m.
Максимальное число
![]() электронов,
находящихся в состояниях, описываемых двумя квантовыми числами n и
электронов,
находящихся в состояниях, описываемых двумя квантовыми числами n и
![]() :
:
![]() =2(2
=2(2![]() +1)
+1)
т. к. m принимает 2![]() +
1 значений,
+
1 значений,
Определим число электронов с определенным
![]() .
.
Электроны с
![]() =0
называются s-электронами, их максимальное количество равно
=0
называются s-электронами, их максимальное количество равно
![]() =
2(2×0+1)=2.
=
2(2×0+1)=2.
Электроны с
![]() =1
называются р-электронами, их максимальное количество равно
=1
называются р-электронами, их максимальное количество равно
![]() =2(2×1+1)=6.
=2(2×1+1)=6.
Электроны с
![]() =2
называются d-электронами, их максимальное количество равно
=2
называются d-электронами, их максимальное количество равно
![]() =2(2
2+1)=10.
=2(2
2+1)=10.
Электроны с ![]() =3
называются f-электронами, их максимальное количество равно
=3
называются f-электронами, их максимальное количество равно
![]() 2(2×3+1)=14 и т.д.
2(2×3+1)=14 и т.д.
Максимальное число
![]() электронов,
находящихся в состояниях, определяемых значением n главного квантового
числа
электронов,
находящихся в состояниях, определяемых значением n главного квантового
числа
![]() =
=![]()
Электроны, занимающие совокупность состояний с
одинаковым значением главного квантового числа n, образуют электронную
оболочку. Различают следующие электронные оболочки (или слои): К-слой при
n
= 1; L-слой
при n
= 2; M-слой
при n
= 3; N-слой
при n
=4 и т.д. В каждой квантовой оболочке атома электроны распределяются по
подоболочкам, соответствующим определенному значению орбитального квантового
числа ![]() ;
в зависимости от
;
в зависимости от ![]() электрон
находится в подгруппе с символами
s,
p,
d,
f
и т.д.
электрон
находится в подгруппе с символами
s,
p,
d,
f
и т.д.
|
Главное квантовое число |
Электронная оболочка (слой) |
Число электронов в состояниях |
Максимальное число электронов |
|||
|
s
( |
p
( |
d
( |
f
( |
|||
|
1 |
K |
2 |
– |
– |
– |
2 |
|
2 |
L |
2 |
6 |
– |
– |
8 |
|
3 |
M |
2 |
6 |
10 |
– |
18 |
|
4 |
N |
2 |
6 |
10 |
14 |
32 |
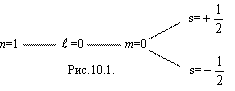 В состоянии, определяемом главным квантовым числом
n
= 1, могут находиться лишь два
s-электрона
с двумя различными ориентациями спинов (см.рис.10.1).
В состоянии, определяемом главным квантовым числом
n
= 1, могут находиться лишь два
s-электрона
с двумя различными ориентациями спинов (см.рис.10.1).
Если n = 2, то схема имеет вид, показанный на рис. 10.2.
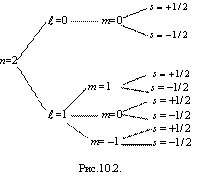 Последовательность заполнения электронных состояний в атомах химических
элементов объясняется принципом Паули.
Последовательность заполнения электронных состояний в атомах химических
элементов объясняется принципом Паули.
Этот принцип дает объяснение периодичности свойств химических элементов в периодической системе, созданной Д.И.Менделеевым.
Принцип Паули позволяет объяснить периодическую повторяемость свойств атомов. В 1869 г. Д.И.Менделеев создал периодическую систему элементов. Он показал, что если элементы расположены по порядку возрастных атомных весов за некоторым исключением, то их физические и химические свойства периодически повторяются. Это сходство распространяется и на их атомные спектры.
По теории Бора такая периодичность в свойствах элементов объясняется тем, что электроны в атомах располагаются по определенным слоям и оболочкам. Электроны, входящие в состав одного слоя, имеют одно и то же главное квантовое число. Оказалось, что каждый период таблицы Менделеева начинается с заполнения электронами нового слоя. Физико-химические свойства элементов (валентность) и оптические свойства определяются числом и расположением самых внешних валентных электронов.
Проследим построение периодической системы (или заполнение электронами слоев атома), которые подчиняются двум принципам: а) заполнение начинается с наименьшей энергии (наиболее устойчивое состояние); б) принцип запрета Паули.
Первый элемент в таблице Менделеева – атом
водорода Н, для него
Z = 1. Он имеет один электрон, квантовые
числа для которого: n
=1, ![]() =
0, mе
= 0, ms
= +1/2 или –1/2, т. е. электронная конфигурация атома водорода: 1S1.
=
0, mе
= 0, ms
= +1/2 или –1/2, т. е. электронная конфигурация атома водорода: 1S1.
У следующего элемента гелия Не имеются два
электрона, квантовые числа:
n =1,
![]() =
0, mе
= 0, ms
= ±1/2,
т. е. электронная конфигурация атома гелия: 1S2.
Слой К с числом электронов N
= 2 заполнен полностью.
=
0, mе
= 0, ms
= ±1/2,
т. е. электронная конфигурация атома гелия: 1S2.
Слой К с числом электронов N
= 2 заполнен полностью.
Третий элемент литий
Li.
Его третий электрон имеет квантовые числа: n = 2,
![]() =
0, mе = 0, ms = +1/2 или – 1/2, т. е. электронная
конфигурация атома 1S2
2S1.
=
0, mе = 0, ms = +1/2 или – 1/2, т. е. электронная
конфигурация атома 1S2
2S1.
У берилия Ве: Z = 4 электронная конфигурация атома 1S2 2S2.
У последующих шести элементов происходит заполнение оболочек 2р. В результате у неона Nе с Z = 10 электронная конфигурация атома 1S2 2S2 2Р6, т.е. L – слой полностью заполнен и на этом заканчивается второй слой периодической таблицы. Не, Nе, а также другие атомы, в которых s- или s- и p-подгруппы полностью заняты электронами, по свойствам аналогичны и химически инертны.
|
Z |
символ элемента |
Название элемента |
Электронная конфигурация |
|
1 |
Н |
водород |
1s1 |
|
2 |
Не |
гелий |
1s2 |
|
3 |
Li |
литий |
1s1 2s1 |
|
4 |
Be |
бериллий |
1s22s2 |
|
5 |
B |
бор |
1s22s22p1 |
|
6 |
C |
углерод |
1s22s22p2 |
|
7 |
N |
азот |
1s22s22p3 |
|
8 |
O |
кислород |
1s22s22p4 |
|
9 |
F |
фтор |
1s22s22p5 |
|
10 |
Ne |
неон |
1s22s22p6 |
|
11 |
Na |
натрий |
1s22s22p63s1 |
|
12 |
Mg |
магний |
1s22s22p63s2 |
|
13 |
Al |
алюминий |
1s22s22p63s23р1 |
|
14 |
Si |
кремний |
1s22s22p63s23р2 |
|
15 |
Р |
фосфор |
1s22s22p63s23р3 |
|
16 |
S |
сера |
1s22s22p63s23р4 |
|
17 |
Cl |
хлор |
1s22s22p63s23р5 |
|
18 |
Ar |
аргон |
1s22s22p63s23р6 |
Нарушения при заполнении слоев наблюдаются у элемента с Z=19 (калий К), где начинается заполнение оболочки 4s при незаполненной 3d:
|
19 |
К |
калий |
1s22s22p63s23р64s1 |
|
20 |
Сa |
кальций |
1s22s22p63s23р64s2 |
|
21 |
Sc |
скандий |
1s22s22p63s23р63d14s2 |
|
22 |
Ti |
титан |
1s22s22p63s23р63d24s2 |
и т.д., пока не будет заполнена 3d-оболочка.
Это нарушение связано с взаимодействием между
электронами, состояние которых характеризуется главными квантовыми числами
n=3,
n=4
и т.д. В результате взаимодействия
возникает такое положение, что
состояние с большим n,
но малым ![]() может
быть энергетически более выгодным.
может
быть энергетически более выгодным.
Аналогичная ситуация наблюдается у редкоземельных элементов, или лантаноидов (атомов с номерами 58-71), у которых заполнены оболочки 5s, 5р, 6s при незаполненной 4f оболочке. У них у всех внешняя оболочка 6s2. Еще одно отступление относится к актиноидам (атомов с номерами 90-103), у которых заполняются 5f оболочка после заполнения внешней оболочки 7s2.
III. ЭЛЕМЕНТЫ ФИЗИКИ ИЗЛУЧЕНИЯ
Из § 11 следует, что оболочки в атомах заполняются электронами последовательно, по мере роста заряда ядра. Внешние (валентные) электроны определяют химические и физические свойства, и они так же отвечают за поглощение и испускание видимого, ультрафиолетового и инфракрасного излучения. Спектры, образованные таким излучением, называются оптическими, поэтому электроны внешних слоев тоже называют оптическими.
С увеличением числа электронов в атоме происходит усложнение спектров. В элементах с высокими атомными номерами ядро слабее действует на внешние электроны, т.к. внутренние электроны экранизируют это действие ядра. Это вызывает усложнение спектров.
Атом излучает только в том случае, если он возбужден. Процесс возбуждения состоит в том, что один или несколько электронов переходит из нормального состояния на внешние, не заполненные, орбиты. Это состояние неустойчиво. Приближенно через t»10-8 с атом возвращается в нормальное положение, излучая при этом квант энергии.
Экспериментально определить распределение электронов по
оболочкам можно по спектрам рентгеновского излучения, длины волн
которого лежат в диапазоне от 8.10–8 до 10–12 м. Для
получения рентгеновского излучения используется рентгеновская трубка. Она
представляет собой баллон (давление в нем порядка 10–6 мм рт.ст.), в
котором находятся электроды: К–катод, А–анод (рис. 12.1).
Источником свободных электронов является катод, нагреваемый
электрическим током и испускающий электроны вследствие явления термоэлектронной
эмиссии. Между катодом и анодом создается ускоряющее электрическое поле.
Электроны в поле приобретают кинетическую энергию
eU,
где
U–
разность потенциалов между катодом и анодом. Попав на анод, электроны
тормозятся при движении в веществе анода. В результате торможения быстрых
электронов возникает тормозное рентгеновское излучение.
Тормозное рентгеновское излучение имеет сплошной непрерывный спектр, который
ограничен со стороны малых длин волн
lmin
– границей сплошного
рентгеновского спектра. С ростом напряжения, подаваемого на трубку, эта граница
смещается в сторону более коротких волн (рис. 12.2). Из соотношения
![]() можно
определить:
можно
определить:
![]() (12.1)
(12.1)
т.е. максимальная энергия
![]() кванта
рентгеновского излучения не может превышать энергию электрона
e=eU,
которую он получил в ускоряющем поле.
кванта
рентгеновского излучения не может превышать энергию электрона
e=eU,
которую он получил в ускоряющем поле.
Кроме тормозного возникает
характеристическое рентгеновское излучение, имеющее линейчатый спектр.
Это название обусловлено тем, что частоты линий спектра являются характерными
для вещества анода. Характеристическое излучение возникает в результате
вырывания электрона с одной из близких к ядру оболочек атома. На освободившееся
место переходит электрон атома из более удаленной от ядра оболочки. Этот
переход сопровождается испусканием кванта рентгеновского излучения, энергией
![]() ,
частота которого определяется зарядом ядра
Ze,
квантовыми числами оболочек, между
которыми совершается переход.
,
частота которого определяется зарядом ядра
Ze,
квантовыми числами оболочек, между
которыми совершается переход.
Электроны, находящиеся ближе к ядру, связаны с ним сильнее, чем внешние. Удалить электрон из внутренней орбиты возможно ударом быстро летящей, посторонней частицы, например, электрона катодных или радиоактивных лучей. В результате этого во внутреннем слое образуется вакантное место, которое занимает один из внешних электронов. При таких переходах электронов из внешнего на внутренний слой излучаются кванты с большой энергией, следовательно, с большой частотой.
Характеристические рентгеновские спектры состоят из линий, объединяющихся в серии. Каждая серия возникает при удалении электрона из какого-либо внутреннего слоя. Эти серии обозначают теми же буквами, что и электронные слои, т. е. К, L, M и т.д. Например, К-серия возникает при переходе электронов на свободные места первого ближайшего к ядру слоя. Схема возникновения рентгеновских спектров дана на рис. 12.3. Каждая серия, в свою очередь, содержит небольшой набор отдельных линий, обозначаемых в порядке убывания длины волны индексами a, b, g, … (Кa, Кb, Кg, …, La, Lb, Lg,…).
Г.Мозли в 1913 установил, что частоты
характеристического спектра элементов возрастают с увеличением порядкового
номера:
![]() (А
– постоянная). Длины волн в спектре характеристического рентгеновского
излучения можно определить по закону Мозли:
(А
– постоянная). Длины волн в спектре характеристического рентгеновского
излучения можно определить по закону Мозли:
![]() ,
,
где R
– постоянная Ридберга, ![]() –
постоянная экранирования;
n1=1,2,3,…
(определяет рентгеновскую серию),
n2
принимает целочисленные значения, начиная с
n1+1
(определяет отдельную линию соответствующей серии).
–
постоянная экранирования;
n1=1,2,3,…
(определяет рентгеновскую серию),
n2
принимает целочисленные значения, начиная с
n1+1
(определяет отдельную линию соответствующей серии).
Смысл постоянной экранирования
![]() заключается
в том, что на электрон, совершающий переход, соответствующий некоторой
линии, действует не весь заряд ядра
Ze,
а заряд (Z–s)e,
ослабленный экранирующим действием других электронов.
заключается
в том, что на электрон, совершающий переход, соответствующий некоторой
линии, действует не весь заряд ядра
Ze,
а заряд (Z–s)e,
ослабленный экранирующим действием других электронов.
Например, для Кa-линии
![]() ,
и закон Мозли запишется в виде:
,
и закон Мозли запишется в виде: ![]() .
.
В
L-серии
для линии La
![]() ,
тогда закон Мозли:
,
тогда закон Мозли: ![]() .
.
Г. Мозли дал объяснение найденного им закона:
линии, длины волн которых определяются по формуле, соответствуют переходам
электрона находящегося в поле заряда
![]() с
уровня с главным квантовым числом
n1
на уровень с номером n2.
Данные результатов исследования Мозли подтвердили, что элементы в таблице
Менделеева расположены в порядке возрастания порядкового номера, то есть заряда
ядра, который может увеличиваться только на единицу.
с
уровня с главным квантовым числом
n1
на уровень с номером n2.
Данные результатов исследования Мозли подтвердили, что элементы в таблице
Менделеева расположены в порядке возрастания порядкового номера, то есть заряда
ядра, который может увеличиваться только на единицу.
Одним из отличий рентгеновских характеристических спектров является то, что не наблюдаются линии поглощения. Объясняется это тем, что при поглощении электрон из внутреннего слоя должен перейти на внешний, не заполненный. Но все ближайшие слои заняты электронами, поэтому квант поглощающей энергии очень велик, значит, длина волны поглощающего света очень мала.
Молекула – наименьшая частица вещества, состоящая из одинаковых или различных атомов, соединенных между собой химическими связями, и являющаяся носителем его основных химических и физических свойств. Химические связи обусловлены взаимодействием внешних, валентных электронов атомов. Наиболее часто в молекулах встречается два типа связи: ионная и ковалентная.
Ионная связь (например, в молекулах NaCl, КВr) осуществляется электростатическим взаимодействием атомов при переходе электрона от одного атома к другому, т.е. при образовании положительного и отрицательного ионов.
Ковалентная связь (например, в молекулах Н2, C2, CO) осуществляется при обобществлении валентных электронов двумя соседними атомами (спины валентных электронов должны быть антипараллельны). Ковалентная связь объясняется на основе принципа неразличимости тождественных частиц, например электронов в молекуле водорода. Неразличимость частиц приводит к обменному взаимодействию.
Молекула является квантовой системой; она описывается уравнением Шредингера, учитывающим движение электронов в молекуле, колебания атомов молекулы, вращение молекулы. Решение этого уравнения – очень сложная задача, которая обычно разбивается на две: для электронов и ядер. Энергия изолированной молекулы:
![]() ,
(13.1)
,
(13.1)
где ![]() –
энергия движения электронов относительно ядер,
–
энергия движения электронов относительно ядер,
![]() –
энергия колебаний ядер (в результате которых периодически изменяется
относительное положение ядер),
–
энергия колебаний ядер (в результате которых периодически изменяется
относительное положение ядер), ![]() –
энергия вращения ядер (в результате которых периодически изменяется ориентация
молекулы в пространстве). В формуле (13.1) не учтены энергия поступательного
движения центра масс молекулы и энергия ядер атомов в молекуле. Первая из них не
квантуется, поэтому ее изменения не могут привести к возникновению молекулярного
спектра, а вторую можно не учитывать, если не рассматривать сверхтонкую
структуру спектральных линий. Доказано, что
–
энергия вращения ядер (в результате которых периодически изменяется ориентация
молекулы в пространстве). В формуле (13.1) не учтены энергия поступательного
движения центра масс молекулы и энергия ядер атомов в молекуле. Первая из них не
квантуется, поэтому ее изменения не могут привести к возникновению молекулярного
спектра, а вторую можно не учитывать, если не рассматривать сверхтонкую
структуру спектральных линий. Доказано, что
![]() эВ,
эВ,
![]() эВ,
эВ,
![]() эВ,
поэтому
эВ,
поэтому ![]() >>
>>![]() >>
>>![]() .
.
Каждая из входящих в выражение (13.1) энергий
квантуется (ей соответствует набор дискретных уровней энергии) и
определяется квантовыми числами. При переходе из одного энергетического
состояния в другое поглощается или испускается энергия
DE=hv.
При таких переходах одновременно
изменяются энергия движения электронов, энергии
колебаний и вращения. Из теории и эксперимента следует, что расстояние между
вращательными уровнями энергии
D![]() гораздо
меньше расстояния между колебательными уровнями
D
гораздо
меньше расстояния между колебательными уровнями
D![]() ,
которое, в свою очередь, меньше расстояния между электронными уровнями
D
,
которое, в свою очередь, меньше расстояния между электронными уровнями
D![]() .
На рисунке 13.1 схематически представлены уровни энергии двухатомной молекулы
(для примера рассмотрены только два электронных уровня – показаны жирными
линиями).
.
На рисунке 13.1 схематически представлены уровни энергии двухатомной молекулы
(для примера рассмотрены только два электронных уровня – показаны жирными
линиями).
Строение молекул и свойства их энергетических уровней проявляются в молекулярных спектрах – спектрах излучения (поглощения), возникающих при квантовых переходах между уровнями энергии молекул. Спектр излучения молекулы определяется структурой ее энергетических уровней и соответствующими правилами отбора.
Итак, при разных типах переходов
между уровнями возникают различные типы молекулярных спектров. Частоты
спектральных линий, испускаемых молекулами, могут соответствовать переходам с
одного электронного уровня на другой (электронные спектры)
или с одного колебательного (вращательного) уровня на другой (колебательные
(вращательные) спектры). Кроме того, возможны и переходы с одними
значениями ![]() и
и
![]() на
уровни, имеющие другие значения всех трех компонентов, в результате чего
возникают электронно-колебательные и колебательно-вращательные спектры.
на
уровни, имеющие другие значения всех трех компонентов, в результате чего
возникают электронно-колебательные и колебательно-вращательные спектры.
Типичные молекулярные спектры – полосатые, представляющие собой совокупность более или менее узких полос в ультрафиолетовой, видимой и инфракрасной областях.
Применяя спектральные приборы высокой разрешающей способности, можно видеть, что полосы представляют собой настолько тесно расположенные линии, что они с трудом разрешаются. Структура молекулярных спектров различна для разных молекул и с увеличением числа атомов в молекуле усложняется (наблюдаются лишь сплошные широкие полосы). Колебательными и вращательными спектрами обладают только многоатомные молекулы, а двухатомные их не имеют. Это объясняется тем, что двухатомные молекулы не имеют дипольных моментов (при колебательных и вращательных переходах отсутствует изменение дипольного момента, что является необходимым условием отличия от нуля вероятности перехода). Молекулярные спектры применяются для исследования строения и свойств молекул, используются в молекулярном спектральном анализе, лазерной спектроскопии, квантовой электронике и т.д.
В 1928 г. Г.С.Ландсберг и Л.И.Мандельштам и одновременно
индийские физики Ч.Раман и К. Кришнан открыли
явление
комбинационного рассеяния света. Если на вещество (газ, жидкость, прозрачный
кристалл) падает строго монохроматический свет, то в спектре
рассеянного света помимо несмещенной
спектральной линии обнаруживаются новые линии, частоты
которых представляют собой суммы или
разности частоты
v падающего света и частот
vi, собственных колебаний (или вращений)
молекул рассеивающей среды: ![]() .
.
Линии в спектре комбинационного рассеяния с частотами v–vi меньшими частоты v падающего света, называются стоксовыми (или красными) спутниками, линии с частотами v + vi, большими vi – антистоксовыми (или фиолетовыми) спутниками.
Исследование спектров комбинационного рассеяния показало, что: 1) линии спутников располагаются симметрично по обе стороны от несмещенной линии; 2) частоты vi не зависят от частоты падающего на вещество света, а определяются только рассеивающим веществом, т.е. характеризуют его состав и структуру; 3) число спутников определяется рассеивающим веществом; 4) интенсивность антистоксовых спутников меньше интенсивности стоксовых и с повышением температуры рассеивающего вещества увеличивается, в то время как интенсивность стоксовых спутников практически от температуры не зависит.
Рассмотрим схему
энергетических уровней молекулы некоторого вещества, в котором наблюдается
комбинационное рассеяние. При освещении светом с частотой
![]() молекула
совершает переход из состояния Е1 в состояние Е2
с поглощением кванта
молекула
совершает переход из состояния Е1 в состояние Е2
с поглощением кванта ![]() .
Из возбужденного состояния молекула может перейти опять в состояние Е1,
что приводит к появлению в спектре рассеянного света линии с «несмещенной»
частотой
.
Из возбужденного состояния молекула может перейти опять в состояние Е1,
что приводит к появлению в спектре рассеянного света линии с «несмещенной»
частотой ![]() (а)
на рис.13.1.) Возможны, однако, и другие пути перехода молекулы в
невозбужденное состояние. Так, молекула
может
сначала перейти в состояние с энергией
(а)
на рис.13.1.) Возможны, однако, и другие пути перехода молекулы в
невозбужденное состояние. Так, молекула
может
сначала перейти в состояние с энергией
![]() ,
где
,
где
![]() –
энергия колебательного или вращательного возбужденного состояния молекулы, а
затем уже перейти в состояние с энергией Е1. Этому переходу
соответствует спектральная линия с частотой:
–
энергия колебательного или вращательного возбужденного состояния молекулы, а
затем уже перейти в состояние с энергией Е1. Этому переходу
соответствует спектральная линия с частотой:
![]() («красный» спутник).
(«красный» спутник).
Из состояния
Е2 молекула за счет обмена энергией с другими молекулами может
перейти в состояние с энергией ![]() ,
оттуда в состояние с энергией Е1:
,
оттуда в состояние с энергией Е1:
![]() («фиолетовый»
спутник).
(«фиолетовый»
спутник).
Рассеяние света может сопровождаться переходами молекулы между различными колебательными или вращательными уровнями, в результате чего и возникает ряд симметрично расположенных спутников. Число спутников, таким образом, определяется энергетическим спектром молекул, т.е. зависит только от природы рассеивающего вещества. Так как число возбужденных молекул гораздо меньше, чем число невозбужденных, то интенсивность антистоксовых спутников меньше, чем стоксовых. С повышением температуры число возбужденных молекул растет, в результате чего возрастам и интенсивность антистоксовых спутников.
С помощью комбинационного рассеяния определяют собственные частоты колебаний молекулы; он позволяет судить о характере симметрии молекулы. С помощью спектров комбинационного рассеяния осуществляют анализ сложных молекулярных смесей.
В силу правил отбора у атомов многих элементов имеются энергетические уровни, с которых электрон не может непосредственно перейти на более низкий уровень. Эти уровни называются метастабильными состояниями. Электрон может перейти на такой уровень при соударениях с другим электроном или при переходе с более высокого уровня. Продолжительность пребывания электрона в метастабильном состоянии имеет порядок 10-–3 с, в то время как в возбужденном состоянии – 10–8 с.
Излучение, испускаемое при самопроизвольном переходе атома из возбужденного состояния в основное, называется спонтанным излучением. Спонтанное излучение различных атомов происходит не когерентно, т.к. каждый атом начинает и заканчивает излучение независимо от других (рис.15.1а).
Излучение энергии атомом, при котором переход из метастабильного состояния в основное вызывается электромагнитным излучением соответствующей частоты называется вынужденным, или индуцированным, излучением (рис.15.1б).
Вероятность индуцированного излучения резко возрастает при совпадении частоты электромагнитного поля с собственной частотой излучения возбужденного атома. Вынужденное излучение имеет такую же частоту, фазу, поляризацию и направление распространения, как и вынуждающее излучение. Следовательно, вынужденное излучение строго когерентно с вынуждающим излучением, то есть испущенный фотон неотличим от фотона, падающего на атом. Испущенные фотоны, двигаясь в одном направлении и встречая другие возбужденные атомы, стимулируют дальнейшие индуцированные переходы, и число фотонов растет лавинообразно.
Однако наряду с вынужденным излучением возможен и конкурирующий процесс – поглощение. В системе атомов, находящейся в термодинамическом равновесии, поглощение падающего излучения будет преобладать над вынужденным, т.е. падающее излучение при прохождении через вещество будет ослабляться.
Чтобы среда усиливала падающее на нее излучение, необходимо создать неравновесное состояние системы, при котором число атомов в возбужденных состояниях было бы больше, чем их число в основном состоянии. Такие состояния называются состояниями с инверсной заселенностью. Процесс создания неравновесного состоянии вещества (перевод системы в состояние с инверсией населенностей) называется накачкой. Накачку можно осуществить оптическими, электрическими и другими способами. Среды с инверсными состояниями называются активными. Их можно рассматривать в качестве сред с отрицательным коэффициентом поглощения, т.к. падающий пучок света при прохождении через эти среды будет усиливаться.
Впервые на возможность получения сред, в которых свет может усиливаться за счет вынужденного излучения, указал в 1939 г. российский физик В.А.Фабрикант. Он экспериментально обнаружил вынужденное излучение паров ртути, возбужденных при электрическом разряде. Открытие явления усиления электромагнитных волн и изобретенный способ их усиления (В.А.Фабрикант, М.М.Вудынский, Ф.А.Бутаева; 1951) легли в основу квантовой электроники, положения которой позволили впоследствии осуществить квантовые усилители и квантовые генераторы света.
Практически инверсное состояние среды осуществлено в оптических квантовых генераторах, или лазерах (от первых букв английского названия Light Amplification by Stimulated Emission of Radiation – усиление света с помощью вынужденного излучения). Лазеры генерируют в видимой, инфракрасной и ближней ультрафиолетовой областях (в оптическом диапазоне). Идея качественно нового принципа усиления и генерации электромагнитных волн, примененная в мазерах (генераторы и усилители, работающие в сантиметровом диапазоне радиоволн) и лазерах, принадлежит российским ученым Н.Г.Басову и А.М.Прохорову и американскому физику Ч. Таунсу, удостоенным Нобелевской премии 1964 г.
Важнейшими из существующих типов лазеров являются твердотельные, газовые, полупроводниковые и жидкостные (в основу такого деления положен тип активной среды). Более точная классификация учитывает также и методы накачки — оптические, тепловые, химические, электроионизационные и др. Кроме того, необходимо принимать во внимание и режим генерации – непрерывный или импульсный.
Лазер обязательно имеет три основных компонента: 1) активную среду, в которой создаются состояния с инверсией населенностей; 2) систему накачки (устройство для создания инверсий в активной среде); 3) оптический резонатор (устройство, выделяющее в пространство избирательное направление пучка фотонов и формирующее выходящий световой пучок).
Первым твердотельным лазером, работающим в видимой области спектра (длина волны излучения 0,6943 мкм), был рубиновый лазер, созданный в 1960 г. (Т.Мейман, США). На рис.16.1 представлена схема рубинового лазера. В нем инверсная населенность уровней осуществляется по трехуровневой схеме, предложенной в 1955 г. Н. Г. Басовым и А. М. Прохоровым. Кристалл рубина представляет собой оксид алюминия А12Оз, в кристаллической решетке которого некоторые из атомов А1 замещены трехвалентными ионами Сгэ+ (0,03 и 0,05% ионов хрома соответственно дня розового и красного рубина). Для оптической накачки используется импульсная газоразрядная лампа (2), спирально закрученная вокруг рубинового стержня (1). При интенсивном облучении рубина светом мощной импульсной лампы атомы хрома переходят с нижнего уровня на уровни широкой полосы 3 (рис. 16.2). Так как время жизни атомов хрома в возбужденных состояниях мало (меньше 10-7 с), то осуществляются либо спонтанные переходы 3®1 (они незначительны), либо наиболее вероятные безызлучательные переходы на уровень 2 (он называется метастабильным) с передачей избытка энергии решетке кристалла рубина. Переход 2®1 запрещен правилами отбора, поэтому длительность возбужденного состояния 2 атомов хрома порядка 10-3 с, т.е. примерно на четыре порядка больше, чем для состояния 3. Это приводит к «накоплению» атомов хрома на уровне 2. При достаточной мощности накачки их концентрация на уровне 2 будет гораздо больше, чем на уровне 1, т. е. возникает среда с инверсной населенностью уровня 2.
Рубиновый стержень лазера представлял собой цилиндр, торцы которого были тщательно отполированы и покрыты слоем серебра таким образом, что один торец полностью отражал свет, а другой – частично отражал и частично пропускал свет. При вспышке лампы накачки в рубиновый стержень попадают фотоны различных частот. Атомы хрома, поглотив часть фотонов определенной энергии, переходят в возбужденное состояние. За счет ограниченных спонтанных переходов в стержне может возникнуть вынужденное излучение, распространяющееся строго вдоль его оси и усиливающееся при многократных отражениях от торцовых зеркал, которые выполняют роль объемного резонатора. В результате возникает мощное монохроматическое излучение – световой импульс, часть которого выходит через полупрозрачное зеркало. Длительность такого импульса 10–3 с. Это связано с тем, что все возбужденные ионы хрома за это время переходят в невозбужденное состояние. Световой луч лазера строго направлен и обладает малой расходимостью. Объемный резонатор лазера служит для создания положительной обратной связи и для формирования геометрических параметров выходного луча лазера.
Не вся энергия, поглощенная рубиновым стержнем, превращается в лазерное излучение. Часть ее, довольно значительная (»50%), тратится на нагревание стержня, поэтому в конструкции лазера предусмотрено охлаждение 3. При температуре стержня порядка 1000 К рубиновый лазер разрушается.
Существует большое количество лазерных материалов: стекло, в которое введены ионы неодима, флюорит кальция с иона ми самария и др. Они дают световое излучение различных длин волн: рубиновый лазер – 0,694 мкм, лазер на стекле с неодимом – 1,06 мкм (инфракрасное излучение). В лазерах в качестве активной среды могут быть использованы газы или смеси газов (Ne, Ar, Ne–Не, СО2 и др.). В газовых лазерах атомы активной среды часто возбуждают высокочастотным разрядом. Как правило, излучение газовых лазеров непрерывно. Созданы полупроводниковые, химические, газодинамические и другие лазеры.
Лазерное излучение обладает следующими свойствами:
1) временная и пространственная когерентность;
2) строгая монохроматичность;
3) большая плотность потока энергии;
4) очень малое угловое расхождение в пучке.
Необычные свойства лазерного излучения нашли широкое применение. Например, в светолучевых станках с помощью лазерного луча делают отверстия в часовых камнях из рубина, алмаза, в тугоплавких сплавах и труднообрабатываемых металлах. В микроэлектронике с помощью лазеров производят сварку различных соединений для микросхем, напыляют полупроводниковые слои и т.д.
IV. ФИЗИКА АТОМНОГО ЯДРА
Э.Резерфорд, исследуя прохождение a-частиц через тонкие пленки золота, пришел к выводу о том, что атом состоит из положительно заряженного ядра и окружающих его электронов. Он также показал, что атомные ядра имеют размеры примерно 10-14–10-15 м (линейные размеры атома примерно 10-10 м).
В 1914 г. Резерфорд провел опыты с водородом. Через трубку, наполненную водородом, пропускали сильные электрические разряды. В результате в трубке оказался заряженный положительно газ. Причем величина заряда этих ионов оказалась равной заряду электрона. Эти положительные ионы являются ядрами атома водорода и были названы протонами. На этом основании было высказано предположение о том, что все ядра содержат протоны, число которых соответствует числу электронов в атоме. На этом основании у следующего за водородом элемента гелия в ядре должно быть два протона, но масса гелия не в два раза больше массы водорода, а в четыре раза больше массы водорода.
Тогда была высказана гипотеза: кроме протонов
ядро содержит частицы, которые не имеют электрического заряда, а масса этой
частицы должна быть приблизительно равна массе протона. Такие частицы были
открыты только через 10 лет, в 1932 г. французские физики И.Кюри и Ф.Жолио-Кюри
провели опыты: они обстреливали ![]() -
частицами бериллий, при этом образовалось неизвестное х – излучение, если
на пути этих лучей поставить новую мишень (они брали на парафин), тогда мы
получаем быстрые протоны. В Англии Джеймс Чедвик повторил этот опыт и доказал,
что излучение, испускаемое бериллием, состоит из частиц, масса которых примерно
равна массе протона и они лишены электрического заряда (
-
частицами бериллий, при этом образовалось неизвестное х – излучение, если
на пути этих лучей поставить новую мишень (они брали на парафин), тогда мы
получаем быстрые протоны. В Англии Джеймс Чедвик повторил этот опыт и доказал,
что излучение, испускаемое бериллием, состоит из частиц, масса которых примерно
равна массе протона и они лишены электрического заряда (![]() )
Эти частицы были названы нейтронами.
)
Эти частицы были названы нейтронами.
После открытия нейтрона возникла протонно-нейтронная модель строения ядра, по которой ядро любого элемента состоит из протонов и нейтронов (протонно-нейтронная модель ядра была предложена российским физиком Д.Д.Иваненко, а впоследствии развита В.Гейзенбергом).
Рассмотрим некоторые характеристики ядер.
Электрический заряд ядра. Ядра всех атомов заряжены положительно. Их заряд определяется числом протонов Z, входящих в состав ядра, и может быть найден по порядковому номеру соответствующего элемента в таблице Менделеева:
![]() ,
(17.1)
,
(17.1)
где
![]() —
заряд ядра, е — положительный заряд, численно равный заряду электрона.
—
заряд ядра, е — положительный заряд, численно равный заряду электрона.
Масса ядра mя. Она не намного отличается от массы атома. Обычно массу ядра измеряют в особых единицах, называемых атомными единицами массы (а. е. м.). За 1 а. е. м. принята 1/12 массы изотопа углерода с массовым числом 12:
1 а.е.м. = (1,66043 ± 0,00031) 10–27 кг.
В качестве примеров приведем массы: протона тр=1,00728 а.е.м., нейтрона тп=1,00867 а. е. м., ядра гелия (a-частицы) тa= 4,00152 а.е.м.
Массовое число А. Это целое число, ближайшее к атомной массе атома, выраженной в а. е. м.
Массовое число равно числу нуклонов в ядре. Таким образом, обозначая число нейтронов в ядре через N, имеем A = Z + N.
Для обозначения ядер используется символическая
запись: ![]() .
X
– химический символ данного элемента.
Нижний индекс у элемента означает
порядковый номер
Z,
верхний –
массовое число А.
.
X
– химический символ данного элемента.
Нижний индекс у элемента означает
порядковый номер
Z,
верхний –
массовое число А.
Некоторые элементы имеют несколько разновидностей, которые отличаются массовым числом, а Z для них постоянно, они называются изотопы.
Например, водород имеет изотопы:
![]() Отсюда
видно, изотопы отличаются содержанием нейтронов в ядре. Еще примеры: кислород:
Отсюда
видно, изотопы отличаются содержанием нейтронов в ядре. Еще примеры: кислород:
![]() ,
уран
,
уран ![]() .
.
Элементы, у которых одинаково массовое число А и
различно Z
называют изобарами. Примерами ядер-изобар могут служить ядра
![]() или
или
![]() ,
,
![]()
Радиус ядра. Первые представления о размере атомного ядра были получены в опытах Резерфорда. Считалось, что ядро соответствует шару с линейным размером порядка 10–12 см. В настоящее время в ядерной физике за единицу длины принимают ферми (1 ферми=10–13 см). В этих единицах имеем
R = (1,45
¸1,5)
![]() .
.
Спин ядра.
Ядро характеризуют спином, который равен сумме спинов
нуклонов.
Спины протона и нейтрона одинаковы и, так же
как у электрона, равны
![]() ,
где
,
где ![]() .
.
Спин ядра, состоящего из четного количества нуклонов, будет
равен
целому числу![]() или
нулю. Например, спин ядра изотопа водорода
или
нулю. Например, спин ядра изотопа водорода
![]() paвен
paвен
![]() , а ядра гелия
, а ядра гелия
![]() –
нулю.
Ядро,
состоящее из нечетного количества нуклонов, имеет спин, равный нечетному числу ½
–
нулю.
Ядро,
состоящее из нечетного количества нуклонов, имеет спин, равный нечетному числу ½![]() .
Например, спин ядра
трития
.
Например, спин ядра
трития![]() равен
½
равен
½![]() ,
а ядра
индия
,
а ядра
индия
![]() –
9
–
9![]() /2.
/2.
Магнитный момент ядра.
Со спином ядра связан магнитный момент рmя.
Обычно его выражают в ядерных магнетонах
mя:
mя=![]() .
.
Магнитный момент протона приближенно равен рmр=2,79mя, а нейтрона рmn = –1, 91mя. Знак “минус” означает, что магнитный момент нейтрона ориентирован противополоңно спину.
Ядро представляет собой прочно связанную систему нуклонов, между которыми действуют ядерные силы. Они имеют весьма короткий радиус действия – порядка 10 см и не зависят от заряда нуклона. Для ядерных сил характерно свойство насыщения, т. е. способность нуклона взаимодействовать не со всеми окружающими его нуклонами, а только с некоторым числом их. Ядерные силы относят к классу сильных взаимодействий: между нуклонами существует притяжение, благодаря которому ядро не распадается, несмотря на электростатическое отталкивание, одноименно заряженных протонов. Эти взаимодействия на много порядков превышают такие силы, как электромагнитные и гравитационные.
Масса ядра меньше суммарной массы всех нуклонов, из которых это ядро состоит. Анализируя известное из теории относительности соотношение, связывающее энергию Е и массу т:
Е = тс2, (18.1)
можно заключить, что и энергия ядра меньше суммарной энергии нуклонов, из которых оно состоит.

Энергию, которую необходимо затратить для того, чтобы расчленить ядро на отдельные составляющие его нуклоны (рис. 18.1), не сообщая им кинетической энергии, называют энергией связи. На основании (18.1) запишем следующее выражение для энергии связи:
![]() (18.2)
(18.2)
Нетрудно убедиться, что атомной единице массы (а. е. м.) соответствует энергия, приблизительно равная 931 МэВ, поэтому формулу (18.2) записывают в виде:
![]() МэВ,
(18.3)
МэВ,
(18.3)
где массы
протона (тр ), нейтрона (тn)
и ядра (mя )
выражены в а.е.м., а
![]() –
в МэВ.
–
в МэВ.
Если учесть, что
![]() ,
то (18.2) примет вид
,
то (18.2) примет вид
![]() .
.
В таблицах обычно приводятся не массы mя ядер, а массы атомов m. Поэтому для энергии связи ядра пользуются формулой
![]() ,
(18.4)
,
(18.4)
где
mН
– масса атома водорода. Так как
![]() (
mэл
– масса электронов), а
(
mэл
– масса электронов), а
![]() , то вычисления по формулам (18.2) и (18.4) приводят к одинаковым
результатам.
, то вычисления по формулам (18.2) и (18.4) приводят к одинаковым
результатам.
Величина
![]() :
:
![]() называется дефектом масс ядра . Она представляет собой разницу
между суммарной массой нуклонов и массой ядра. На эту величину уменьшается масса
всех нуклонов при образовании из них атомного ядра.
называется дефектом масс ядра . Она представляет собой разницу
между суммарной массой нуклонов и массой ядра. На эту величину уменьшается масса
всех нуклонов при образовании из них атомного ядра.
Часто вместо энергии связи рассматривают удельную энергию связи. Удельной энергией связи называется энергия связи, приходящаяся на один нуклон:
![]()
![]() МэВ.
МэВ.
На рис. 18.2. показана зависимость
![]() от
массового числа А различных ядер. Для легких ядер (А£12)
удельная энергия связи круто возрастает до 6¸7
МэВ (например, для
от
массового числа А различных ядер. Для легких ядер (А£12)
удельная энергия связи круто возрастает до 6¸7
МэВ (например, для ![]()
![]() =1,1
МэВ, для
=1,1
МэВ, для ![]()
![]() =7,6
МэВ, претерпевая целый ряд скачков, затем более медленно возрастает до
максимальной величины 8,7 МэВ у элементов с А=50¸60,
а потом постепенно уменьшается у тяжелых элементов (например, для
=7,6
МэВ, претерпевая целый ряд скачков, затем более медленно возрастает до
максимальной величины 8,7 МэВ у элементов с А=50¸60,
а потом постепенно уменьшается у тяжелых элементов (например, для
![]() она
составляет 7,6 МэВ).
она
составляет 7,6 МэВ).
Уменьшение удельной энергии связи при переходе к тяжелым элементам объясняется тем, что с возрастанием числа протонов в ядре увеличивается и энергия их кулоновского отталкивания. Поэтому связь между нуклонами становится менее сильной, а сами ядра менее прочными.
Наиболее
устойчивыми оказываются так называемые магические ядра, у которых
число протонов или число нейтронов равно одному из
магических чисел: 2, 8, 20, 28, 50,
82, 126. Особенно стабильны дважды магические ядра,
у которых магическими являются
и число протонов, и число нейтронов. Этих ядер насчитывается всего пять:
![]() .
.
Из рис. 18.2 следует, что наиболее устойчивыми с энергетической точки зрения являются ядра средней части таблицы Менделеева. Тяжелые и легкие ядра менее устойчивы. Это означает, что энергетически выгодны следующие процессы: 1) деление тяжелых ядер на более легкие; 2) слияние легких ядер друг с другом в более тяжелые. При обоих процессах выделяется огромное количество энергии; эти процессы в настоящее время осуществлены практически: реакции деления и термоядерные реакции.
Нуклоны в ядре удерживаются за счет особых сил, называемых ядерными. Ядерное взаимодействие получило название сильного взаимодействия, т.к. эти силы в миллионы раз превышают силы электромагнитного взаимодействия.
Основные свойства ядерных сил:
1) ядерные силы являются силами притяжения;
2)
ядерные силы являются
короткодействующими – их действие проявляется на расстояниях![]() ;
;
3) ядерные силам свойственна зарядовая независимость – ядерные силы, действующие между двумя протонами, или двумя нейтронами, или между протоном и нейтроном, одинаковы по величине. Значит, ядерные силы имеют неэлектрическую природу;
4) ядерные силы не являются центральными – не действуют вдоль линии, соединяющей центры частиц;
5)
ядерные силы зависят от взаимной
ориентации спинов нуклонов. Например, протон и нейтрон удерживаются вместе,
образуя ядро тяжелого водорода ![]() , только в том случае, если их спины параллельны друг другу;
, только в том случае, если их спины параллельны друг другу;
6) ядерные силы обладают свойством насыщения – это означает, что каждый нуклон взаимодействует не со всеми остальными, а с ограниченным числом нуклонов. Насыщение проявляется в том, что удельная энергия связи нуклонов в ядре при увеличении числа нуклонов не растет, а остается приблизительно постоянной.
Как известно из электродинамики, взаимодействие
между заряженными частицами осуществляется посредством электромагнитного поля.
Такое поле можно представить как совокупность фотонов с энергией
hv,
тогда взаимодействие двух заряженных частиц можно объяснить обменом фотонами.
Например, ![]() -
взаимодействие между электронами. Причем, эти фотоны являются виртуальными,
т.е. их нельзя обнаружить за время взаимодействия между частицами.
-
взаимодействие между электронами. Причем, эти фотоны являются виртуальными,
т.е. их нельзя обнаружить за время взаимодействия между частицами.
В 1934 г. И.Е.Тамм высказал предположение, что взаимодействие между нуклонами также осуществляется посредством каких-то виртуальных частиц. В 1935 г. японский физик Юкава высказал гипотезу о том, в ядрах протоны и нейтроны с чудовищной быстротой как бы обменивается частицами, которые обладают массой, в 200-300 раз большей, чем электрон. Позднее эти частицы назвали «мезонами». В 1947 г. в космических лучах обнаружили частицы, которые назвали p-мезоны (пионы). Строение нуклона в настоящее время представляется следующим.
В центре нуклонов находится ядро-керн, радиус которого 0,3×10–15 м.
Керн окружен
«облаком», состоящим из мезонов. Носителями ядерных
сил являются
p-мезоны,
или пионы; существуют положительный (p+), отрицательный (p–) и нейтральный (p0) мезоны. Время жизни
p+-
и
p–-мезонов равно 2,6
× 10–8 с, а
p0-мезона
– 0,8× 10–16 с.
Массовые числа
![]() .
В результате виртуальных
процессов, т.е. процессов, которые не могут
быть обнаружены за время их протекания, происходят следующие
превращения:
.
В результате виртуальных
процессов, т.е. процессов, которые не могут
быть обнаружены за время их протекания, происходят следующие
превращения:
![]() ;
;
![]() ;
;
![]() ;
;
![]()
Эти предположения подтвердились на опытах по рассеиванию нейтронов на ядрах водорода.
Модели ядра. Для описания поведения ядер пользуются различными теориями. Одним из методов изучения свойств атомного ядра является метод моделей ядра. Метод моделей основан на внешней аналогии свойств атомного ядра со свойствами соответствующей модели. Ядерные модели можно разделить на группы: капельная, оболочечная, обобщенная, оптическая и др. Ни одна из существующих моделей не может дать исчерпывающего ответа обо всех свойствах атомного ядра и характеризует лишь определенные его свойства. Каждую модель используют при рассмотрении определенного круга ядерных процессов. Наиболее распространенными из них являются две: капельная и оболочечная.
1. Капельная модель ядра (1936; Н.Бор и Я.И.Френкель). Эта модель основана на аналогии между поведением нуклона в ядре и поведением молекул в капле жидкости:
- ядерные силы между нуклонами и сила взаимодействия между молекулами в жидкости имеют малый радиус действия, т.е. являются короткодействующими;
- ядерные силы обладают свойством насыщения: каждый нуклон, как и каждая молекула в капле, взаимодействует только с ограниченным числом нуклонов, а не со всеми нуклонами ядра;
- плотность ядерного вещества приблизительно постоянна и не зависит от числа нуклонов, входящих в ядро. И для капли жидкости при данных внешних условиях характерна постоянная плотность ее вещества;
- ядерные частицы, как и молекулы жидкости, обладают определенной подвижностью;
- энергия притяжения нуклонов в ядре аналогична энергии межмолекулярного взаимодействия в капле жидкости. С увеличением числа протонов, входящих в ядро, энергия связи уменьшается за счет действия кулоновских сил, что соответствует снижению устойчивости капли жидкости с увеличением числа молекул в капле;
- нуклоны, находящиеся на «поверхности» ядра, испытывают силы, аналогичные силам поверхностного натяжения, действующим на молекулу жидкости, находящуюся на ее поверхности;
- при возбуждении ядра энергия распределяется между нуклонами статистическим образом подобно тому, как распределяется энергия, передаваемая жидкости при ее нагревании.
Существенное отличие ядра от капли жидкости в этой модели заключается в том, что она трактует ядро как каплю электрически заряженной несжимаемой жидкости (с плотностью, равной ядерной), подчиняющуюся законам квантовой механики. Капельная модель объяснила механизм ядерных реакций и особенно реакции деления ядер. Она допускает изменение формы ядра при сохранении объема. Это может привести к делению капли-ядра на части. Однако эта модель не смогла, например, объяснить повышенную устойчивость ядер, содержащих магические числа протонов и нейтронов.
2.
Оболочечная модель
(1949-1950; американский физик М.Гепперт-Майер
и немецкий физик
X.Иенсен).
Оболочечная модель предполагает распределение нуклонов в ядре по дискретным
энергетическим уровням (оболочкам), заполняемым нуклонами согласно принципу
Паули, и связывает устойчивость ядер с заполнением этих уровней.
Расстояние между уровнями порядка МэВ. При
переходе с одного уровня на другой происходит излучение
g-квантов.
Считается, что ядра с полностью заполненными оболочками являются наиболее устойчивыми. Такие особо
устойчивые (магические)
ядра действительно существуют (например, дважды магические ядра –
![]()
![]() ).
Оболочечная модель ядра позволила объяснить спины и
магнитные моменты ядер, различную устойчивость атомных ядер, а также
периодичность изменений их свойств.
Эта модель особенно хорошо применима для
описания легких и средних ядер, а также для ядер, находящихся в основном
(невозбужденном) состоянии.
).
Оболочечная модель ядра позволила объяснить спины и
магнитные моменты ядер, различную устойчивость атомных ядер, а также
периодичность изменений их свойств.
Эта модель особенно хорошо применима для
описания легких и средних ядер, а также для ядер, находящихся в основном
(невозбужденном) состоянии.
Французский физик А. Беккерель в 1896 г. при изучении люминесценции солей урана случайно обнаружил самопроизвольное испускание ими излучения неизвестной природы, которое действовало на фотопластинку, ионизировало воздух, проникало сквозь тонкие металлические пластинки, вызывало люминесценцию ряда веществ. Беккерель показал, что все соединения урана обладают свойством самопроизвольного излучения, и интенсивность этого излучения зависит от содержания в соединении урана. Это излучение не зависит от температуры в интервале от – 2000 С до +2000 С.
Продолжая исследование этого явления, супруги Кюри – Мария
и Пьер –
обнаружили, что беккерелевское излучение свойственно не только урану, но
и многим другим
тяжелым элементам, таким, как торий и актиний. Они показали
также, что
урановая смоляная обманка (руда, из которой добывается металлический
уран) испускает
излучение, интенсивность которого во много раз превышает интенсивность
излучения урана. Им удалось выделить два новых элемента – носителя
беккерелевского излучения: полоний ![]() и
радий
и
радий ![]() .
.
Обнаруженное излучение было названо радиоактивным излучением, а само явление – испускание радиоактивного излучения – радиоактивностью. Дальнейшие опыты показали, что радиоактивные свойства элемента обусловлены структурой его ядра.
В настоящее время под радиоактивностью понимают способность некоторых атомных ядер самопроизвольно превращаться в другие ядра с испусканием различных видов радиоактивных излучений и элементарных частиц. Радиоактивность подразделяется на естественную (наблюдается у неустойчивых изотопов, существующих в природе) и искусственную (наблюдается у изотопов, полученных посредством ядерных реакций). Принципиального различия между этими двумя типами радиоактивности нет, так как законы радиоактивного превращения в обоих случаях одинаковы.
Работу по исследованию явления радиоактивности
продолжил Резерфорд, который поставил задачу выяснить природу радиоактивных
лучей. Для этого он использовал метод отклонений в магнитном поле.
Оказалось, что излучение, даваемое радиоактивным веществом, в магнитном поле
разделяется на три компонента. Они были названы ![]() лучи.
лучи.
a-Излучение
отклоняется электрическим и магнитным полями, обладает высокой
ионизирующей способностью и
малой проникающей способностью (например, поглощаются слоем алюминия толщиной примерно 0,05 мм).
a-Излучение
представляет собой поток ядер
гелия; заряд a-частицы равен +2е, а масса совпадает с массой
ядра изотопа гелия ![]() .
Скорость a-частиц
.
Скорость a-частиц
![]() м/с.
м/с.
b-Излучение
отклоняется электрическим и магнитным полями; его ионизирующая
способность
значительно меньше (примерно на два порядка), а проникающая способность
гораздо больше (поглощается слоем алюминия толщиной примерно 2 мм), чем
у
a-частиц.
b-Излучение представляет собой поток
быстрых электронов, скорость которых
![]() .
Оно сильно рассеивается в веществе.
.
Оно сильно рассеивается в веществе.
g-Излучение не отклоняется электрическим и магнитным полями, обладает относительно слабой ионизирующей способностью и очень большой проникающей способностью (например, проходит через слой свинца толщиной 5 см), при прохождении через кристаллы обнаруживает дифракцию. g-Излучение представляет собой коротковолновое электромагнитное излучение с чрезвычайно малой длиной волны l<10-10 м и вследствие этого – ярко выраженными корпускулярными свойствами, т.е. является потоком частиц – g-квантов (фотонов).
К 1904 г. Резерфорд остановился на том, что радиоактивность – это распад нестабильных атомов, при котором атом, испуская радиоактивные лучи, превращается в новый нестабильный атом. Этот процесс продолжается до тех пор, пока не возникает стабильный нерадиоактивный атом. К этому времени были измерены массы ядер многих элементов и установили, что эта масса зависит от места элемента в таблице Менделеева.
Под радиоактивным распадом, или просто распадом, понимают естественное радиоактивное превращение ядер, происходящее самопроизвольно. При радиоактивном превращении происходит изменение строения и состава исходного ядра, причем это изменение определяется внутриядерными процессами. Атомное ядро, испытывающее радиоактивный распад, называется материнским, возникающее ядро – дочерним.
В основе теории радиоактивного распада лежит предположение, что этот процесс происходит самопроизвольно, является следствием неустойчивости ядер и подчиняется статистическим законам. Вероятность того, что отдельный нестабильный атом испытывает радиоактивное превращение в единицу времени, со временем не изменяются, но различна для разных атомов.
Так как отдельные радиоактивные ядра распадаются независимо друг от друга, то можно считать, что число ядер dN, распавшихся в среднем за интервал времени от t до t+dt, пропорционально промежутку времени dt и числу N нераспавшихся ядер к моменту времени t:
![]() ,
(21.1)
,
(21.1)
где
![]() -
постоянная для данного радиоактивного вещества, называемая постоянной
радиоактивного распада. Знак минус указывает, что число нераспавшихся ядер
со временем убывает.
-
постоянная для данного радиоактивного вещества, называемая постоянной
радиоактивного распада. Знак минус указывает, что число нераспавшихся ядер
со временем убывает.
Разделим переменные в (21.1):
![]() и
проинтегрируем полученное выражение:
и
проинтегрируем полученное выражение:
![]() ;
;
![]() .
Тогда:
.
Тогда:
![]() ,
(21.2)
,
(21.2)
где N0 – начальное число нераспавшихся ядер (в момент времени t=0), N – число нераспавшихся ядер в момент времени t. Формула (21.2) выражает закон радиоактивного распада, согласно которому число нераспавшихся ядер убывает со временем по экспоненциальному закону.
Интенсивность процесса радиоактивного распада
характеризуют две величины: период полураспада
![]() и
среднее время жизни. Период полураспада
и
среднее время жизни. Период полураспада
![]() –
промежуток времени, в течение которого число радиоактивных ядер в среднем
уменьшается вдвое. Тогда, согласно (21.2),
–
промежуток времени, в течение которого число радиоактивных ядер в среднем
уменьшается вдвое. Тогда, согласно (21.2),
![]() ,
откуда:
,
откуда: ![]() .
.
Для разных элементов этот промежуток времени
различен. Для радия Ra:
![]() =1590
лет; для радона Rn:
=1590
лет; для радона Rn:
![]() =3,8
дня.
=3,8
дня.
Суммарная продолжительность жизни dN ядер равна:
![]() .
Чтобы получить среднее время жизни
t,
проинтегрируем это выражение по всем возможным
t
и разделим на начальное число ядер:
.
Чтобы получить среднее время жизни
t,
проинтегрируем это выражение по всем возможным
t
и разделим на начальное число ядер:
![]() .
.
Итак, среднее время жизни
t
радиоактивного ядра есть величина, обратная постоянной радиоактивного распада
l:
![]() .
.
Активность радиоактивного элемента определяет число ядер, распавшихся за единицу времени:
![]() .
.
Единица активности в СИ – беккерель (Бк): 1 Бк – активность ядра, при которой за 1 с происходит один акт распада.
Радиоактивный распад происходит в соответствии с законами сохранения массового числа и электрического заряда. Эти законы позволяют установить «правила смещения», по которым можно определить, какой элемент возникает в результате радиоактивного превращения.
a-Распад.
Превращение атомных ядер, сопровождаемых испусканием
a-частиц
(ядер атомов гелия ![]() ),
называется a-распадом.
Если символом
),
называется a-распадом.
Если символом ![]() обозначить
материнское ядро, то превращение этого ядра при
a-распаде
происходит по схеме:
обозначить
материнское ядро, то превращение этого ядра при
a-распаде
происходит по схеме:
![]() ,
(22.1)
,
(22.1)
где
![]() –
символ дочернего ядра;
–
символ дочернего ядра; ![]() –
g-квант, испускаемый ядром
–
g-квант, испускаемый ядром ![]() ,
находящимся в возбужденном состоянии. Как видно из (22.1),
a-распад
уменьшает массовое число на 4, а заряд ядра – на 2 элементарных положительных
заряда, то есть происходит перемещение химического элемента на две клетки
влево в периодической системе элементов Менделеева. Например,
,
находящимся в возбужденном состоянии. Как видно из (22.1),
a-распад
уменьшает массовое число на 4, а заряд ядра – на 2 элементарных положительных
заряда, то есть происходит перемещение химического элемента на две клетки
влево в периодической системе элементов Менделеева. Например, ![]() .
.
Процесс a-распада состоит из двух стадий: образования a-частицы в ядре атома и испускания ее ядром. Устойчивость виртуального образования из двух протонов и двух нейтронов есть следствие насыщения ядерных сил. На образовавшуюся a-частицу в ядре действуют как ядерные силы притяжения, так и кулоновские силы отталкивания. Образовавшаяся a-частица подвержена меньшему действию ядерных сил, но большему действию кулоновских сил, чем отдельные протоны, входящие в состав a-частицы.
![]() –Распад. Исследования показали, что радиоактивные ядра могут
выбрасывать поток электронов. Массовое число при
b-распаде не изменяется, а зарядовое число увеличивается на единицу:
–Распад. Исследования показали, что радиоактивные ядра могут
выбрасывать поток электронов. Массовое число при
b-распаде не изменяется, а зарядовое число увеличивается на единицу:
![]() .
.
Следовательно, новый химический элемент
перемещается на одну клеточку вправо в периодической системе
Менделеева. Раз не изменяется
массовое число, следовательно, не должен
изменяться суммарный спин всех нуклонов в
ядре, но электрон, обладающий спином
![]() ,
должен изменять спин ядра. Однако при
b-распаде
не происходит изменения спина ядра. В.Паули предположил, что вместе с электроном
из ядра должна вылететь еще одна частица, получившая название нейтрино (v).
Она не имеет заряда и массы покоя, но должна иметь спин,
равный спину электрона
,
должен изменять спин ядра. Однако при
b-распаде
не происходит изменения спина ядра. В.Паули предположил, что вместе с электроном
из ядра должна вылететь еще одна частица, получившая название нейтрино (v).
Она не имеет заряда и массы покоя, но должна иметь спин,
равный спину электрона
![]() .
При одновременном вылете из ядра электрона
и нейтрино возможно, что их спины ориентированы во взаимно противоположных
направлениях, поэтому суммарный спин ядра не изменяется.
.
При одновременном вылете из ядра электрона
и нейтрино возможно, что их спины ориентированы во взаимно противоположных
направлениях, поэтому суммарный спин ядра не изменяется.
По современным представлениям, существует три
разновидности
b-распада:
электронный (b–-распад); позитронный (b+-распад);
К-захват. Частица, испускаемая при позитронном распаде, называется нейтрино
(v),
а при электронном – антинейтрино (![]() ).
).
b–-распад протекает по схеме:
![]() .
.
Например, по теории Ферми, в ядре возможны
превращения нуклонов, в результате которых появляются электроны и антинейтрино:
![]() .
.
b+-распад протекает по схеме: ![]() ,
,
где ![]() –позитрон.
Этот вид распада возможен тогда, когда в ядре один из протонов превращается в
нейтрон. В результате появляется позитрон и нейтрино:
–позитрон.
Этот вид распада возможен тогда, когда в ядре один из протонов превращается в
нейтрон. В результате появляется позитрон и нейтрино:
![]() .
На протекание этой реакции затрачивается энергия, так как масса нейтрона больше
массы протона.
.
На протекание этой реакции затрачивается энергия, так как масса нейтрона больше
массы протона.
В случае К-захвата (или электронного захвата) возбужденное ядро захватывает электрон К-оболочки атома, при этом один из протонов ядра превращается нейтрон и возникает нейтрино:
![]() .
.
В случае К-захвата происходит испускание характеристического рентгеновского излучения.
Ядерными реакциями называется искусственное превращение атомных ядер при их взаимодействии как друг с другом, так и с ядерными частицами, в результате чего образуются новые ядра и новые частицы. Символически ядерную реакцию можно записать:
![]() или
или
![]() (23.1),
(23.1),
где Х и У – исходное и конечное ядра, а и b – исходная и конечная частицы в реакции.
Ядерная реакция характеризуется энергией
ядерной реакции ![]() , равной разности кинетических энергий частиц, полученных в
результате реакции и кинетических энергий частиц, участвующих в реакции
, равной разности кинетических энергий частиц, полученных в
результате реакции и кинетических энергий частиц, участвующих в реакции ![]() (23.2).
(23.2).
Если ![]() ,
реакция происходит с поглощением энергии и называется эндотермической;
если
,
реакция происходит с поглощением энергии и называется эндотермической;
если ![]() ,
то реакция идет с выделением энергии, реакция называется экзотермической.
В ядерных реакциях выполняются законы сохранения энергии, импульса,
электрического заряда и массовых чисел. Если применить закон сохранения масс и
энергий для ядерной реакции, то можно записать:
,
то реакция идет с выделением энергии, реакция называется экзотермической.
В ядерных реакциях выполняются законы сохранения энергии, импульса,
электрического заряда и массовых чисел. Если применить закон сохранения масс и
энергий для ядерной реакции, то можно записать:
![]() (23.3),
(23.3),
где ![]() - энергия покоя частиц или ядер.
- энергия покоя частиц или ядер.
Из (23.2) и (23.3) следует:
![]() (23.4)
(23.4)
Поэтому условие экзотермической реакции (![]() )
выполняется. если
)
выполняется. если ![]() ,
а эндотермической (
,
а эндотермической (![]() ),
если
),
если ![]() .
Таким образом, в отличие от радиоактивного распада, который протекает всегда с выделением
энергии, ядерные реакции могут быть как экзотермическими, так и
эндотермическими.
.
Таким образом, в отличие от радиоактивного распада, который протекает всегда с выделением
энергии, ядерные реакции могут быть как экзотермическими, так и
эндотермическими.
Важную роль в объяснении механизма многих ядерных реакций сыграло предположение Н. Бора (1936) о том, что ядерные реакции протекают в две стадии по следующей схеме:
X+а ®C®Y+b. (23.5)
Первая стадия – это захват ядром X частицы а, приблизившейся к нему на расстояние действия ядерных сил (примерно 2×10-15 м), и образование промежуточного ядра С, называемого составным, которое оказывается в возбужденном состоянии. При столкновении нуклонов составного ядра один из нуклонов или a-частица может получить энергию, достаточную для вылета из ядра. В результате возможна вторая стадия ядерной реакции – распад составного ядра на ядро Y и частицу b.
Некоторые реакции протекают без образования составного ядра, они называются прямыми ядерными взаимодействиями.
Ядерные реакции классифицируются по следующим признакам:
1) по роду участвующих в них частиц – реакции под действием нейтронов; реакции под действием заряженных частиц; реакции под действием g-квантов;
2) по энергии вызывающих их частиц – реакции при малых энергиях (порядка 1 эВ), происходящие в основном с участием нейтронов; реакции при средних энергиях (до нескольких МэВ), происходящие с участием g-квантов и заряженных частиц (протоны, a-частицы); реакции при высоких энергиях (сотни и тысячи МэВ), приводящие к рождению отсутствующих в свободном состоянии элементарных частиц и имеющие большое значение для их изучения;
3) по роду участвующих в них ядер – реакции на легких ядрах (А<50); реакции на средних ядрах (50<А<100); реакции на тяжелых ядрах (А> 100);
4) по характеру происходящих ядерных превращений – реакции с испусканием нейтронов; реакции с испусканием заряженных частиц; реакции захвата.
Первая в истории ядерная реакция осуществлена Э.Резерфордом (1919) при бомбардировке ядра азота a-частицамн, испускаемыми радиоактивным источником:
![]() .
.
Другой пример ядерных реакций – реакция получения нейтронов (предсказана и доказана Д.Чэдвигом в 1932 г.):
![]() .
.
Наиболее распространенными ядерными реакциями являются реакции деления тяжелых ядер и синтеза легких. Рассмотрим их более подробно.
Реакция деления ядер урана при бомбардировке их нейтронами была открыта в 1939 г. Было установлено, что при облучении урана нейтронами образуются элементы из середины периодической таблицы – лантан и барий. При делении одного ядра урана освобождается около 200 МэВ энергии: на кинетическую энергию движения ядер-осколков приходится примерно 165 МэВ, остальную энергию уносят g-кванты. Выход энергии при делении всех ядер 1 кг урана составляет 80 тысяч миллиардов джоулей. Это в несколько миллионов раз больше, чем энергия, которая выделяется при сжигании 1 кг каменного угля или нефти.
Деление ядер сопровождается испусканием двух-трех
вторичных нейтронов, называемых нейтронами деления. В среднем на один акт
деления приходится 2,5 нейтронов. Среди нейтронов деления имеются
мгновенные
(возникшие через 10-14 с) и запаздывающие нейтроны.
Образовавшиеся осколки деления перегружены нейтронами, в результате чего они и
выделяют нейтроны деления. Однако испускание нейтронов деления не устраняет
полностью перегрузку ядер-осколков нейтронами. Это приводит к тому, что осколки
также могут претерпеть ряд
b––превращений,
сопровождаемых испусканием
g-квантов, после которых образуется стабильный изотоп. Например, при
делении ядра урана ![]() :
:
![]() (24.1)
(24.1)
осколок деления ![]() в
результате трех актов
b––распада
превращается в стабильный изотоп лантана
в
результате трех актов
b––распада
превращается в стабильный изотоп лантана
![]() :
:
![]() .
.
Осколки деления могут быть разнообразными,
поэтому реакция (24.1) не единственная приводящая к делению урана
![]() .
Возможны, например, реакции:
.
Возможны, например, реакции:
![]() или
или
![]()
Кроме урана под действием нейтронов делятся атомы
![]() ,
протактиния
,
протактиния ![]() ,
плутоний
,
плутоний ![]() .
Причем ядра урана
.
Причем ядра урана ![]() ,
плутония
,
плутония ![]() делятся
под действием нейтронов с любой энергией, но особенно хорошо под действием
медленных (или тепловых) нейтронов, энергия которых порядка 1МэВ. Ядра же
делятся
под действием нейтронов с любой энергией, но особенно хорошо под действием
медленных (или тепловых) нейтронов, энергия которых порядка 1МэВ. Ядра же
![]() делятся
только быстрыми нейтронами, энергия которых может иметь значения от
нескольких МэВ до 50 МэВ.
делятся
только быстрыми нейтронами, энергия которых может иметь значения от
нескольких МэВ до 50 МэВ.
В основу теории деления атомных ядер (Н.Бор, Я.И.Френкель) положена капельная модель ядра. Ядро рассматривается как капля электрически заряженной несжимаемой жидкости, частицы которой при попадании нейтрона в ядро приходят в колебательное движение, в результате чего ядро разрывается на две части, разлетающиеся с огромной энергией.
Испускание мгновенных нейтронов при делении тяжелых ядер делает возможной цепную реакцию. Каждый из мгновенных нейтронов, возникающих в реакции деления, взаимодействуя с соседними ядрами делящегося вещества, вызывает реакцию деления. При этом идет лавинообразное нарастание числа актов деления, которое также объясняется на основе капельной модели строения ядра.
Впервые предложение о возможности осуществления цепных ядерных реакций высказал Ф.Жолио-Кюри в 1934 г. Он же в 1939 г. вместе с Халбаном и Л.Коварски экспериментально обнаружил, что при делении ядра урана, кроме осколков ядер, вылетают также 2-3 свободных нейтрона.
Условием возникновения цепной реакции является наличие размножающихся нейтронов. Коэффициентом размножения нейтронов k называется отношение числа нейтронов, возникающих в некотором звене реакции, к некоторому числу таких нейтронов в предшествующем звене. Необходимым условием для развития цепной реакции деления является требование k³1.
Коэффициент размножения зависит от природы делящегося вещества, а для данного изотопа – от его количества, а также размеров и формы активной зоны. Активной зоной называется пространство, где происходит цепная реакция. Минимальные размеры активной зоны, при которых возможно осуществление цепной реакции, называются критическими размерами. Минимальная масса делящегося вещества, находящегося в системе критических размеров, необходимая для осуществления цепной реакция, называется критической массой.
Скорость развития цепных реакций
различна. Пусть Т – среднее время жизни
одного поколения, а N – число
нейтронов в данном поколении. В следующем поколении
их число равно
kN,
т. е. прирост числа нейтронов за одно
поколение
dN–kN–N=N(k–1).
Прирост же числа нейтронов за единицу времени, т. е. скорость
нарастания цепной реакции:
![]() .
Проинтегрировав это выражение, получим:
.
Проинтегрировав это выражение, получим:
![]()
где N0 — число нейтронов в начальный момент времени, а N – их число в момент времени t. N определяется знаком (k –1). При k>1 идет развивающаяся реакции, число делений непрерывно растет и реакция может стать взрывной. При k = 1 идет самоподдерживающаяся реакция, при которой число нейтронов с течением времени не изменяется. При k < 1 идет затухающая реакция.
Цепные реакции делятся на
управляемые и неуправляемые. Взрыв атомной бомбы,
например, является неуправляемой реакцией. Чтобы атомная бомба при
хранении не взорвалась, в ней
![]() (или
(или
![]() )
делится на две удаленные друг от друга части
с массами ниже критических. Затем с помощью
обычного взрыва эти массы сближаются, общая масса делящегося вещества
становится больше критической и возникает взрывная цепная реакция,
сопровождающаяся мгновенным выделением огромного
количества энергии и большими разрушениями.
Взрывная реакция начинается за счет
имеющихся нейтронов спонтанного деления или нейтронов космического излучения.
Использовать энергию ядерного взрыва в мирных целях очень трудно, т.к.
выделение энергии при этом не поддается контролю. Управляемые цепные реакции
деления ядер урана осуществляется в ядерных реакторах.
)
делится на две удаленные друг от друга части
с массами ниже критических. Затем с помощью
обычного взрыва эти массы сближаются, общая масса делящегося вещества
становится больше критической и возникает взрывная цепная реакция,
сопровождающаяся мгновенным выделением огромного
количества энергии и большими разрушениями.
Взрывная реакция начинается за счет
имеющихся нейтронов спонтанного деления или нейтронов космического излучения.
Использовать энергию ядерного взрыва в мирных целях очень трудно, т.к.
выделение энергии при этом не поддается контролю. Управляемые цепные реакции
деления ядер урана осуществляется в ядерных реакторах.
В ядерных реакторах используется реакция, идущая
с постоянной интенсивностью, при этом
k=1.
В реактор вводятся вещества, ядра которых
могут поглощать нейтроны. Таким образом получают радиоактивные искусственные
изотопы и искусственное ядерное горючее. Первые реакторы строились для
получения плутония, затем появились
исследовательские реакторы и, наконец, энергетические. Главная задача
энергетических реакторов – превращение ядерной энергии в
электрическую. Наиболее перспективный путь
развития атомной энергетики – разработка реакторов на быстрых нейтронах. Такой
реактор производит больше ядерного горючего, чем потребляет. Реакция идет на
быстрых нейтронах, поэтому в ней могут
участвовать не только ![]() и
и
![]() ,
но и
,
но и ![]() .
В активную зону загружается ядерное горючее, обогащенное
.
В активную зону загружается ядерное горючее, обогащенное
![]() или
или
![]() .
Вместо отражателя активная зона окружается зоной воспроизводства, в
которую загружают
.
Вместо отражателя активная зона окружается зоной воспроизводства, в
которую загружают ![]() .
Таким образом, для получения энергии
реакторы на быстрых нейтронах позволяют использовать весь уран (
.
Таким образом, для получения энергии
реакторы на быстрых нейтронах позволяют использовать весь уран (![]() и
и
![]() ),
а также торий
),
а также торий ![]() ,
который, как и
,
который, как и ![]() ,
делится только быстрыми нейтронами, что
намного увеличивает ресурсы ядерного горючего.
,
делится только быстрыми нейтронами, что
намного увеличивает ресурсы ядерного горючего.
Ядерная энергия освобождается не только в ядерных
реакциях деления тяжелых ядер, но и в реакциях соединения легких атомных ядер.
Удельная энергия связи ядер резко увеличивается при переходе от ядер тяжелого
водорода (![]() ,
,
![]() )
к литию
)
к литию ![]() и
к гелию
и
к гелию ![]() ,
т.е. реакции синтеза легких ядер в более тяжелые должны сопровождаться
выделением большого количества энергии. В качестве примеров можно привести
следующие реакции синтеза:
,
т.е. реакции синтеза легких ядер в более тяжелые должны сопровождаться
выделением большого количества энергии. В качестве примеров можно привести
следующие реакции синтеза:
![]() (Q=4,0
МэВ);
(Q=4,0
МэВ);
![]() (Q=3,3
МэВ);
(Q=3,3
МэВ);
![]() (Q=17,6
МэВ);
(Q=17,6
МэВ);
![]() (Q=22,4
МэВ),
(Q=22,4
МэВ),
где Q – энерговыделение.
Для соединения одноименно заряженных протонов
необходимо преодолеть кулоновские силы отталкивания, что возможно при достаточно
больших скоростях сталкивающихся частиц. Синтез гелия из легкого изотопа
водорода происходит при температурах
![]() К,
а для синтеза гелия из тяжелых изотопов водорода дейтерия и трития – по схеме
К,
а для синтеза гелия из тяжелых изотопов водорода дейтерия и трития – по схеме
![]() требуется
нагревание примерно до
требуется
нагревание примерно до ![]() К.
К.
Реакция синтеза легких атомных ядер в более
тяжелые, происходящие при сверхвысоких температурах, называются термоядерными
реакциями. Термоядерные реакции дают наибольший выход энергии на единицу
массы «топлива». Например, при синтезе 1 г гелия из дейтерия и трития
выделяется энергия ![]() Дж.
Такая энергия выделяется при сжигании 10 тонн дизельного топлива.
Дж.
Такая энергия выделяется при сжигании 10 тонн дизельного топлива.
Необходимые условия для синтеза ядер гелия имеются в недрах Солнца и других звезд. Термоядерные реакции являются одним из источников энергии этих светил. На Земле термоядерная реакция синтеза осуществлена при экспериментальных термоядерных взрывах. В 1953 г. в нашей стране, через полгода – в США были произведены испытания водородной бомбы, где взрывчатым веществом служила смесь дейтерия и трития, а запалом – атомная бомба, при взрыве которой возникает необходимая для протекания реакции температура. В этом случае реакция термоядерного синтеза является неуправляемой.
Особый интерес представляет осуществление управляемой термоядерной реакции. Для обеспечения управляемой термоядерной реакции необходимо создание и поддержание в ограниченном объеме температуры порядка 108 К. При данной температуре термоядерное рабочее вещество представляет собой полностью ионизованную плазму, поэтому возникает проблема ее термоизоляции от стенок установки, в которой она находится. Для того чтобы удержать ее от соприкосновения со стенками установки, в настоящее время применяется магнитная термоизоляция. Так как плазма состоит из заряженных частиц, то в сильном магнитном поле на заряженную частицу действует сила Лоренца, вследствие чего траектория частицы винтообразно навивается на силовую линию.
В 1975 году в Институте атомной энергии под
руководством Л.А.Арцимовича был пущен крупнейший в мире термоядерный реактор
«Токамак-10» (Т-10). В Т-10 плазма создается в тороидальной камере, находящейся
в магнитном поле, а само плазменное образование – плазменный шнур – также имеет
форму тора. На этой установке удалось получить плазму с температурой
![]() и
плотностью n=1014
частиц/см3 и поддержать ее в течение
t=1
с. Однако для получения условия, необходимого для начала самоподдерживающейся
термоядерной реакции, нужно примерно в 20 раз увеличить
nt
(произведение плотности
частиц на время удержания плазмы) и примерно в 10 раз температуру.
и
плотностью n=1014
частиц/см3 и поддержать ее в течение
t=1
с. Однако для получения условия, необходимого для начала самоподдерживающейся
термоядерной реакции, нужно примерно в 20 раз увеличить
nt
(произведение плотности
частиц на время удержания плазмы) и примерно в 10 раз температуру.
До более высоких температур водород может быть нагрет с помощью лазерного излучения. В экспериментах на лазерных установках уже получена плазма с температурой в несколько десятков миллионов градусов. Запасы водорода на Земле практически неисчерпаемые, поэтому использование энергии термоядерного синтеза в мирных целях является одной из важнейших задач современной науки и техники.
V. ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
Развитие физики элементарных частиц тесно связано с изучением космического излучения – ионизирующего излучения, приходящего из потока приходящих извне частиц.
Различают первичное и вторичное космическое излучение.
Излучение, приходящее непосредственно из космоса, называют первичным космическим излучением. Исследование его состава показало, что первичное излучение представляет собой поток протонов (более 90%), ядер атомов гелия (около 7%) и атомов более тяжелых элементов с Z>20 (около 1%), движущихся со скоростями, близкими к скорости света. Энергия большинства частиц лежит в пределах от 109 до 1012 эВ. При h>50 км интенсивность космического излучения постоянна; на этих высотах наблюдается лишь первичное излучение.
Вторичное космическое излучение образуется в результате взаимодействия первичного космического излучения с ядрами атомов земной атмосферы. Во вторичном космическом излучении встречаются практически все известные элементарные частицы. На высотах ниже 20 км космическое излучение является вторичным; с уменьшением h его интенсивность понижается вследствие поглощения.
В околоземном пространстве существуют области, в которых интенсивность потока заряженных частиц, захваченных магнитным полем Земли, превышает интенсивность первичного потока космического излучения в сотни миллионов раз. Эти области названы радиационными поясами. Установлено, что радиационный пояс Земли представляет собой единое образование. Внутренняя граница радиационного пояса в плоскости экватора находится на расстоянии 600 км от поверхности Земли в западном полушарии и около 1600 км в восточном. Внешняя граница пояса в плоскости экватора находится на расстоянии 8–10 радиусов Земли. Несимметричное расположение радиационного пояса Земли объясняется тем, что движение заряженных частиц определяется структурой магнитного поля Земли.
В составе вторичного космического излучения можно выделить два компонента: мягкий (сильно поглощается свинцом) и жесткий (обладает в свинце большой проникающей способностью).
Мягкая компонента состоит из каскадов, или ливней электронно-позитронных пар. Образовавшийся при ядерном взаимодействии или торможении быстрого электрона g-фотон, пролетая вблизи атомного ядра, создает пару электрон-позитрон с высокой кинетической энергией (рис.27.1). Торможение этих частиц приводит к появлению новых g-фотонов, которые образуют новые пары и т. д. Процессы рождения пар и возникновения g-квантов чередуются друг с другом до тех пор, пока энергия g-фотонов не станет недостаточной для образования новых пар. Поскольку энергия первоначального фотона бывает очень большой, успевает возникнуть много поколений вторичных частиц, прежде чем прекращается развитие ливня.
Жесткая компонента космических лучей состоит в основном из мюонов. Ее образование происходит преимущественно в верхних и средних слоях атмосферы за счет распада заряженных p-мезонов.
Исследование космического излучения, с одной стороны, позволило на начальном этапе развития физики элементарных частиц получить основные экспериментальные данные, на которых базировалась эта область науки, а с другой – дало возможность и сейчас изучать процессы с частицами сверхвысоких энергий вплоть до 1021 эВ, которые еще не получены искусственным путем. С начала 50-х гг. для исследования элементарных частиц стали применять ускорители, в связи с чем космическое излучение утратило свою исключительность при их изучении, оставаясь источником получения информации из мирового пространства.
Элементарные частицы в точном значении этого термина – первичные, неделимые частицы, из которых состоит вся материя. Понятие “элементарная частица” трансформировалась по мере развития знаний о строении материи. На рубеже XIX-XX веков мельчайшей частицей вещества (т.е. элементарной частицей) считался атом (по-гречески atomos - ”неделимый”). В дальнейшем выявилась сложная структура атома, состоящего из ядра и электронов. В свою очередь ядра, как оказалось, также являются сложными структурами и состоят из протонов и нейтронов. В настоящее время считается, что протоны и нейтроны также состоят из более элементарных частиц – кварков. В строгом смысле именно кварки в настоящее время должны считаться элементарными частицами. Однако в современной физике термин “элементарные частицы” употребляется не в своем точном значении, а менее строго – для наименования большой группы мельчайших частиц материи, которые не являются атомами или атомными ядрами, т.е. объектами заведомо составной природы. В эту группу входят протон (p), нейтрон (n), фотон (g ), p - мезоны и другие частицы – всего более 350 частиц, в основном нестабильных.
Японский физик X. Юкава, изучая природу ядерных сил, выдвинул в 1935 г. гипотезу о существовании частиц с массой, в 200-300 раз превышающей массу электрона. Эти частицы должны выполнять роль носителей ядерного взаимодействия, подобно тому, как фотоны являются носителями электромагнитного взаимодействия.
К. Андерсон и С. Неддермейер, изучая поглощение жесткого компонента вторичного космического излучения в свинцовых фильтрах, действительно обнаружили (1936) частицы массой, близкой к ожидаемой (207me). Они были названы впоследствии мюоамн. Доказано, что жесткий компонент вторичного космического излучения состоит в основном из мюнов, которые, как будет показано ниже, образуются вследствие распада более тяжелых заряженных частиц (p- и K-мезонов).
Существуют положительный (m+) и отрицательный (m–) мюоны; заряд мюонов равен элементарному заряду е. Масса мюонов равна 206,8 те, время жизни m+- и m–-мюонов одинаково и равно 2,2×10–6 с. Исследования показали, что мюоны претерпевают самопроизвольный распад, являясь, таким образом, нестабильными частицами. Распад мюонов происходит по следующим схемам:
![]() (28.1)
(28.1)
![]() (28.2)
(28.2)
где ![]() и
и
![]() –
соответственно «мюнные» нейтрино и антинейтрино, которые
отличаются от
–
соответственно «мюнные» нейтрино и антинейтрино, которые
отличаются от ![]() и
и
![]() –
«электронных» нейтрино и антинейтрино, сопутствующих испусканию
позитрона и электрона соответственно. Существование
–
«электронных» нейтрино и антинейтрино, сопутствующих испусканию
позитрона и электрона соответственно. Существование
![]() и
и
![]() следует из законов сохранения энергии и
спина.
следует из законов сохранения энергии и
спина.
Из схем распада (28.1) и (28.2)
следует, что спины мюонов, как и электрона, должны быть равны 1/2 (в
единицах ![]() ),
так как спины нейтрино (1/2) и антинейтрино
(–1/2) взаимно компенсируются.
),
так как спины нейтрино (1/2) и антинейтрино
(–1/2) взаимно компенсируются.
Дальнейшие эксперименты привели к выводу, что мюоны не взаимодействуют с атомными ядрами, то есть являются ядерно-неактивными частицами. Мюоны, с одной стороны, из-за ядерной пассивности не могут рождаться при взаимодействии первичного компонента космического излучения с ядрами атомов атмосферы, а с другой – из-за нестабильности не могут находиться в составе первичного космического излучения. Следовательно, отождествить мюоны с частицами, которые, согласно X.Юкаве, являлись бы носителями ядерного взаимодействия, не удалось, так как такие частицы должны интенсивно взаимодействовать с ядрами. Это привело к выводу о том, что должны существовать какие-то ядерно-активные частицы, распад которых и приводит к образованию мюонов. Действительно, в 1947 г. была обнаружена частица, обладающая свойствами, предсказанными Юкавой, которая распадается на мюон и нейтрино. Этой, частицей оказался p-мезон.
Английский физик С. Пауэлл и его сотрудники, подвергая на большой высоте ядерные фотоэмульсии действию космических лучей (1947), обнаружили ядерно-активные частицы так называемые p-мезоны (от греч. «мезос» — средний), или пионы. Тогда же пионы были получены искусственно в лабораторных условиях при бомбардировке мишеней из Be, С и Сu a-частицами, ускоренными в синхроциклотроне до 300 МэВ. p-Мезоны сильно взаимодействуют с нуклонами и атомными ядрами и, по современным представлениям, обусловливают существование ядерных сил.
Существуют положительный (p+), отрицательный (p–) (их заряд равен элементарному заряду е) и нейтральный (p0) мезоны. Масса p+ и p–-мезонов одинакова и равна 273,1те, масса p0-мезона равна 264,1те. Все пионы нестабильны: время жизни соответственно для заряженных и нейтрального p-мезонов составляет 2,6×10–8 и 0,8 ×10–16 с. Распад заряженных пионов происходит в основном по схемам:
![]() ;
(28.3)
;
(28.3)
![]() (28.4)
(28.4)
где мюоны испытывают дальнейший
распад по рассмотренным выше схемам (28.1) и
(28.2). Из схем распада (28.3) и (28.4) следует, что спины заряженных
p-мезонов
должны быть либо
целыми (в единицах
![]() ),
либо равны нулю. Спины заряженных
p-мезонов, по ряду других
экспериментальных данных, оказались равными нулю. Нейтральный пион распадается
на два
g-кванта:
),
либо равны нулю. Спины заряженных
p-мезонов, по ряду других
экспериментальных данных, оказались равными нулю. Нейтральный пион распадается
на два
g-кванта:
![]() .
Спин
p0-мезона,
так же как и спин
p+-мезона,
равен нулю.
.
Спин
p0-мезона,
так же как и спин
p+-мезона,
равен нулю.
Исследования в космических лучах методом фотоэмульсий (1949) и изучение
реакций с участием частиц высоких энергий, полученных на ускорителях, привели к
открытию К-мезонов, или каонов, – частиц с нулевым спином и с массами,
приблизительно равными 970 те.
В настоящее время известно четыре типа каонов: положительно
заряженный (К+), отрицательно
заряженный (К– ) и два нейтральных (К0 и
![]() 0).
Время жизни К-мезонов лежит в пределах 10–8–10–10
с в зависимости от их типа.
0).
Время жизни К-мезонов лежит в пределах 10–8–10–10
с в зависимости от их типа.
Существует несколько схем распада К-мезонов. Распад заряженных К-мезонов происходит преимущественно по схемам:

Распад нейтральных К-мезонов в основном происходит по следующим схемам (в порядке убывания вероятности распада):
для
короткоживущих (![]() )
)
![]() ;
;
для долгоживущих
(![]() )
)

Различные процессы с элементарными частицами заметно различаются по интенсивности их протекания. В соответствии с этим взаимодействия элементарных частиц можно разделить на четыре класса: сильное, электромагнитное, слабое и гравитационное.
Сильное взаимодействие вызывает процессы, протекающие с наибольшей интенсивностью, оно приводит к самой сильной связи элементарных частиц. Именно это взаимодействие обуславливает связь протонов и нейтронов в ядрах атомов и обеспечивает устойчивость ядер. Потому сильное взаимодействие называют также ядерным.
Электромагнитное взаимодействие осуществляется через электрическое поле. Это взаимодействие возможно только между электрически заряженными телами. Электромагнитное взаимодействие заметно слабее сильного. Именно это взаимодействие обуславливает связь электронов с ядром в атоме и атомов в молекуле.
Слабое взаимодействие вызывает очень медленно протекающие процессы с элементарными частицами. Примером процесса, обусловленного слабым взаимодействием, является b-распад и m-распад, а примером элементарной частицы, способной только к слабому взаимодействию, может служить нейтрино. Именно крайне малой интенсивностью слабого взаимодействия объясняется тот факт, что нейтрино свободно пронизывают толщу Земли и Солнца, не испытывая при этом поглощения.
Гравитационное взаимодействие является универсальным, оно наблюдается между любыми материальными телами, но в микромире оно не играет существенной роли. По сравнению с остальными тремя взаимодействиями оно пренебрежимо мало.
Приведем ряд характеристик перечисленных взаимодействий:
|
Тип взаимодействия |
Механизм обмена |
Сравнительная величина интенсивности взаимодействия |
Радиус действия сил, м. |
Длительность протекания процесса, с |
|
Сильное |
глюонами |
1 |
10-15 |
10-23 |
|
Электромагнитное |
фотонами |
10-2 … 10-3 |
¥ |
10-20 |
|
Слабое |
промежуточными бозонамии |
10-10 … 10-14 |
10–18 |
10-10 |
|
Гравитационное |
гравитонами |
10-38 … 10-40 |
¥ |
|
По способности к тому или иному виду взаимодействия все элементарные частицы делятся на три группы:
1) фотоны; эта группа состоит всего лишь из одной частицы –фотона – кванта электромагнитного излучения;
2) лептоны (or греч. «лептос»- легкий), участвующие только в электромагнитном и слабом взаимодействиях. К лептонам относятся электронное и мюонное нейтрино, электрон, мюон и открытый в 1975 г. тяжелый лептон – t-лептон, или таон, с массой примерно 3487me, а также соответствующие им античастицы. Название лептонов связано с тем, что массы первых известных лептонов были меньше масс всех других частиц. К лептонам относится также таонное нейтрино, существование которого в последнее время также установлено;
3) адроны (от греч. «адрос» — крупный, сильный). Адроны обладают сильным взаимодействием наряду с электромагнитным и слабым. К ним относятся также протон, нейтрон, пионы, каоны и гипероны.
Для всех типов взаимодействия элементарных частиц выполняются законы сохранения энергии, импульса, момента импульса и электрического заряда.
Каждой из элементарных частиц, за небольшим исключением, соответствует своя античастица. Масса покоя, спин, время жизни и некоторые другие характеристики у частиц и античастиц одинаковы. Электрические заряды и магнитные моменты частицы и античастицы равны по величине, но противоположны по знаку. Однако наличие электрического заряда не является обязательным условием существования пары частица – античастица. Кроме разноименных электрических зарядов, частицы и античастицы имеют противоположные знаки барионного заряда (барионы и антибарионы) и лептонного заряда (лептоны и антилептоны).
В качестве примеров уже рассмотренных частиц и античастиц можно указать на электрон и позитрон (антиэлектрон), протон и антипротон, нейтрон и антинейтрон, p + и p –– мезоны, нейтрино и антинейтрино. Частицами, не имеющими античастиц, являются, например, фотон или p 0- мезон. Такие частицы принято называть истинно нейтральными. Нейтрон, например, хотя и не имеет электрического заряда, не является истинно нейтральной частицей, так как он имеет античастицу – антинейтрон, отличающийся знаком барионного заряда В (В = +1 для нейтрона и В = -1 для антинейтрона).
При соединении частицы и античастицы (этот процесс называется аннигиляцией) выделяется энергия, равная, как минимум, суммарной энергии покоя частицы и античастицы. Для рождения пары частица – античастица требуется энергия, превышающая суммарную энергию покоя пары частиц, так как родившимся частицам необходимо сообщить импульс (иначе они тут же аннигилируют), а следовательно, и кинетическую энергию.
Кроме способности к различным взаимодействиям, элементарные частицы имеют другие характеристики, прежде всего массу, время жизни, спин, электрический заряд.
По массе все частицы делятся на тяжелые – адроны, средние – мезоны, легкие – лептоны.
В зависимости от времени жизни элементарные частицы делятся на стабильные, квазистабильные и нестабильные (резонансы). Стабильными, в пределах точности современных измерений, являются электрон (t > 5×1021 лет), протон (t > 2×1030 лет), фотон и нейтрино. К квазистабильным относят частицы, распадающиеся за счёт электромагнитных и слабых взаимодействий. Их времена жизни > 10-20 сек (для свободного нейтрона даже ~ 1000 сек). Резонансами называются элементарные частицы, распадающиеся за счёт сильных взаимодействий. Их характерные времена жизни 10-23–10-24 с.
Спин может быть целым или полуцелым кратным величине
![]() .
В этих единицах спин
p-
и К-мезонов равен 0, у протона, нейтрона и электрона J= 1/2, у фотона
J = 1. Существуют частицы и с более высоким спином. Величина спина
элементарной частицы определяет поведение ансамбля одинаковых (тождественных)
частиц, или их статистику (В.Паули,
1940). Частицы полуцелого спина подчиняются статистике
Ферми-Дирака
(отсюда название
фермионы),
которая требует антисимметрии
волновой функции
системы относительно перестановки пары частиц (или нечётного числа пар) и,
следовательно, «запрещает» двум частицам полуцелого спина находиться в
одинаковом состоянии (принцип
Паули).
Частицы целого спина подчиняются статистике
Бозе-Эйнштейна
(отсюда название
бозоны),
которая требует симметрии волновой функции относительно перестановок частиц
и допускает нахождение любого числа частиц в одном и том же состоянии.
Статистические свойства элементарных частиц оказываются существенными в тех
случаях, когда при рождении или распаде образуется несколько одинаковых частиц.
.
В этих единицах спин
p-
и К-мезонов равен 0, у протона, нейтрона и электрона J= 1/2, у фотона
J = 1. Существуют частицы и с более высоким спином. Величина спина
элементарной частицы определяет поведение ансамбля одинаковых (тождественных)
частиц, или их статистику (В.Паули,
1940). Частицы полуцелого спина подчиняются статистике
Ферми-Дирака
(отсюда название
фермионы),
которая требует антисимметрии
волновой функции
системы относительно перестановки пары частиц (или нечётного числа пар) и,
следовательно, «запрещает» двум частицам полуцелого спина находиться в
одинаковом состоянии (принцип
Паули).
Частицы целого спина подчиняются статистике
Бозе-Эйнштейна
(отсюда название
бозоны),
которая требует симметрии волновой функции относительно перестановок частиц
и допускает нахождение любого числа частиц в одном и том же состоянии.
Статистические свойства элементарных частиц оказываются существенными в тех
случаях, когда при рождении или распаде образуется несколько одинаковых частиц.
Статистика Ферми-Дирака играет также исключительно важную роль в структуре ядер и определяет закономерности заполнения электронами атомных оболочек, лежащие в основе периодической системы элементов Д.И.Менделеева.
Электрические заряды изученных элементарных частиц является целым кратным величине е=1,6.10-19 Кл (элементарный электрический заряд). У известных элементарных частиц Q = 0, ±1, ±2.
Классификация самых распространенных элементарных частиц приведена в таблице.
Таблица. Классификация элементарных частиц.
|
Группа |
Название частицы |
Символ |
Заряд, ед.е |
Масса покоя, ед. me |
Спин, ћ |
Время жизни, с |
Лепт. число L |
Барион.число В |
Странность, S |
||
|
частицы |
анти-частицы |
||||||||||
|
Фотоны |
Фотон |
g |
0 |
0 |
1 |
Стаби-лен |
0 |
0 |
0 |
||
|
Лептоны |
Электрон |
e- |
e+ |
1 |
1 |
1/2 |
Стаби-лен |
+1 |
0 |
0 |
|
| Электронное нейтрино |
|
|
0 |
0 |
1/2 |
Стаби-льно |
+1 |
0 |
0 |
||
| Мюон |
|
|
1 |
206,8 |
1/2 |
»10–6 |
+1 |
0 |
0 |
||
|
Мюонное нейтрино |
|
|
0 |
0 |
1/2 |
Стаби-льно |
+1 |
0 |
0 |
||
|
Таон |
t– |
t+ |
1 |
3487 |
½ |
»10–12 |
+1 |
0 |
0 |
||
|
Таонное нейтрино |
|
|
0 |
0 |
½ |
? |
+1 |
0 |
0 |
||
|
Адроны |
Мезоны |
Пионы |
p 0 p + |
p – |
0 1 |
264,1 273,1 |
0 0 |
»10–16 »10–8 |
0 0 |
0 0 |
0 0 |
|
Каоны |
|
|
0 1 |
974,0 966,2 |
0 0 |
10–10-10–8 »10–8 |
0 0 |
0 0 |
+1 +1 |
||
|
Барионы |
Протон |
|
|
1 |
1836,2 |
½ |
Стаби-лен |
0 |
+1 +1 |
0 |
|
|
Нейтрон |
|
|
0 |
1838,7 |
½ |
»103 |
0 |
0 |
0 |
||
|
Гипероны: лямбда
сигма
кси
омега |
|
|
0 0 1 1 0 1
1 |
2183 2334 2328 2343 2573 2586 3273 |
1/2 1/2 1/2 1/2 1/2 1/2 3/2 |
»10–10 »10–20 »10–10 »10–10 »10–10 »10–10 »10–10 |
0 0 0 0 0 0 0 |
+1 +1 +1 +1 +1 +1
+1 |
-1 -1 -1 -1 -1 -1 -1 |
||
Помимо указанных величин, элементарные частицы характеризуются еще рядом квантовых чисел, называемых внутренними. Лептоны несут специфический лептонный заряд L двух типов: электронный (Le) и мюонный (Lm); Le = +1 для электрона и электронного нейтрино, Lm= +1 для отрицательного мюона и мюонного нейтрино. Тяжёлый лептон (таон) и связанное с ним нейтрино, по-видимому, являются носителями нового типа лептонного заряда Lt.
Для адронов L = 0, и это ещё одно проявление их отличия от лептонов. В свою очередь, значительные части адронов следует приписать особый барионный заряд В (|В| = 1). Адроны с В = +1 образуют подгруппу барионов (сюда входят протон, нейтрон, гипероны, барионные резонансы), а адроны с В = 0 – подгруппу мезонов (p- и К-мезоны, бозонные резонансы). Название подгрупп адронов происходит от греческих слов barýs – тяжёлый и mésos – средний, что на начальном этапе исследований элементарных частиц отражало сравнительные величины масс известных тогда барионов и мезонов. Более поздние данные показали, что массы барионов и мезонов сопоставимы. Для лептонов В = 0. Для фотона В=0 и L=0.
Барионы и мезоны подразделяются на уже упоминавшиеся совокупности: обычных (нестранных) частиц (протон, нейтрон, p-мезоны), странных частиц (гипероны, К-мезоны) и очарованных частиц. Этому разделению отвечает наличие у адронов особых квантовых чисел: странности S и очарования (английское charm) Ch с допустимыми значениями: |S| = 0, 1, 2, 3 и |Ch| = 0, 1, 2, 3. Для обычных частиц S = 0 и Ch = 0, для странных частиц |S|¹0, Ch = 0, для очарованных частиц |Ch|¹0, а |S| = 0, 1, 2.
Квантовые числа элементарных частиц разделяются на точные, которые связаны с физическими величинами, сохраняющимися во всех процессах, и неточные, для которых соответствующие физические величины в некоторых процессах не сохраняются. Точными квантовыми числами являются: электрический заряд q, лептонный заряд L и барионный заряд B, спин. Странность S, очарование Сh и красота b – неточные квантовые числа, они сохраняются в сильных и электромагнитных взаимодействиях, но не сохраняются в слабом взаимодействии.
Уже первые исследования с обычными адронами выявили наличие среди них семейств частиц, близких по массе, с очень сходными свойствами по отношению к сильным взаимодействиям, но с различными значениями электрического заряда. Протон и нейтрон (нуклоны) были первым примером такого семейства. Позднее аналогичные семейства были обнаружены среди странных и (в 1976) среди очарованных адронов. Общность свойств частиц, входящих в такие семейства, является отражением существования у них одинакового значения специального квантового числа – изотопического спина I, принимающего, как и обычный спин, целые и полуцелые значения. Сами семейства обычно называются изотопическими мультиплетами. Число частиц в мультиплете (п) связано с I соотношением: n = 2I + 1. Частицы одного изотопического мультиплета отличаются друг от друга значением «проекции» изотопического спина I3 .
Важной характеристикой адронов является также внутренняя чётность Р, связанная с операцией пространственной инверсии: Р принимает значения ±1.
Для процессов взаимопревращаемости элементарных частиц, обусловленных сильными взаимодействиями, выполняются все законы сохранения (энергии, импульса, заряда (электрического, лептонного, барионного), изоспина, странности и четности. В процессах, обусловленных слабым взаимодействием, не сохраняются только изоспин, странность и четность.
Классификация элементарных частиц начала интенсивно развиваться с середины 50-х годов ХХ в. Были предприняты попытки потсроить все известные элементарные частицы из небольшого числа составных частей. Такие попытки предпринимали Юкава и Гейзенберг. Первый реальный успех в деле классификации элементарных частиц выпал на долю М.Гелл-Манна и Дж.Цвейга, показавших, что все известные к 1964 г. барионы и мезоны можно составить из трех фундаментальных частиц– кварков. У названия «кварк» нет точного перевода, оно имеет литературное происхождение (было заимствовано М. Гелл-Маном из романа Дж. Джойса «Поминки по Финегану», где означало нечто неопределённое, мистическое). Такое название для частиц, очевидно, было выбрано потому, что кварку необходимо приписать ряд необычных свойств, выделяющих их из всех известных элементарных частиц (например, дробный электрический заряд). Согласно кварковой модели, все известные тогда адроны можно было построить, постулируя существование трех типов кварков (u, d, s) и соответствующих антикварков (u, d, s).
После 1964 года были открыты новые барионы и мезоны, для классификации которых оказалось недостаточно этих трех кварков. В настоящее время к трем первоначальным кваркам добавлены еще три: общее число кварков возросло до 6. Чтобы различать эти 6 кварков, ученые наделили кварки свойством, которое они назвали «аромат». Разумеется, запаха кварки не имеют, но считается, что каждый из 6 кварков «пахнет» по-своему, имеет свой особый «аромат». Три кварка, введенные М. Гелл-Маном и Дж.Цвейгом, имели ароматы «вверх» (u – up), «вниз» (d–down) и «странность» (s – strange). Другие кварки имели ароматы «очарованный» (с – charm), «истинный» (t – truth), «прелестный» (b – beauty). Вот некоторые характеристики кварков:
|
|
Час- |
Электри- |
Бари- |
Спин J |
Cтран- S |
|
Кварки |
u d s с t b |
+2/3 –1/3 –1/3 +2/3 +2/3 –1/3 |
1/3 1/3 1/3 1/3 |
1/2 1/2 1/2 1/2 |
0 0 –1 0 0 0 |
|
Антикварки |
|
–2/3 +1/3 +1/3 –2/3 –2/3 +1/3 |
-1/3 -1/3 -1/3 -1/3 |
1/2 1/2 1/2 1/2 |
0 0 +1 0 0 0 |
Кроме того, существуют три кварка каждого аромата, отличающихся квантовым число, называемым цветом и принимающим три значения – желтый, синий, красный. Каждому кварку соответствует антикварк, имеющий по отношению к данному кварку противоположный электрический заряд и так называемый антицвет: антижелтый, антисиний, антикрасный. Таким образом, принимая во внимание число ароматов и цветов, получается 36 кварков и антикварков.
Кварки взаимодействуют друг с другом посредством обмена восемью глюонами, которые представляют собой безмассовые бозоны со спином 1. Кварк, входящий в состав адрона, испускает глюон, в силу чего состояние движения адрона изменяется. Этот глюон поглощается кварком, входящим в состав другого адрона, и меняет состояние его движения. В результате возникает взаимодействие адронов друг с другом. Комбинации кварков, составляющих элементарные частицы, таковы, что наблюдается бесцветный образ. Отличительная особенность кварк-кваркового взаимодействия через глюоны состоит в том, что с уменьшением расстояния их взаимодействие ослабляется. Это ведет к тому, что внутри адронов кварки можно рассматривать как свободные частицы. Имеются убедительные экспериментальные доказательства их существования в связанном состоянии внутри адронов. Кваркам выгодно находиться внутри адронов. Это означает, что возможно наблюдать только бесцветные адроны. Одиночные кварки, будучи цветными объектами, не могут существовать в свободном состоянии, а могут находиться только внутри белых частиц – адронов. Как следствие, для отделения кварков друг от друга требуется бесконечно большая энергия.
Мезоны состоят из пары кварка-антикварк
(символически ![]() );
а барионы – из трех кварков, символически
);
а барионы – из трех кварков, символически
![]() .
Кварковый состав некоторых адронов приведен в следующей таблице:
.
Кварковый состав некоторых адронов приведен в следующей таблице:
|
Мезоны |
Барионы |
||||||
|
p + |
p - |
p 0 |
К+ |
Протон p |
Нейтрон n |
S+-гиперон |
S0-гиперон |
|
|
|
|
|
|
|
|
|
В отличие от барионов и мезонов лептоны в настоящее время рассматриваются как элементарные частицы в буквальном смысле слова как не имеющие внутренней структуры. Интересно, что число видов лептонов (их шесть) совпадает с числом кварков, если три цвета одного и того же кварка рассматривать как одну частицу. Является ли схема из шести лептонов и шести кварков окончательной или же число лептонов (кварков) будет расти, покажут дальнейшие исследования.